Hvad er navnene og kemiske formler for fem forbindelser, hvor Krypton eksisterer?
1. krypton difluorid (KRF2) :Dette er den mest kendte og stabile forbindelse af Krypton. Det er et farveløst, flygtigt fast stof.
2. krypton tetrafluorid (KRF4) :Dette er en mindre stabil forbindelse end KRF2 og dannes kun under ekstreme forhold.
3. krypton hexafluorid (krf6) :Denne forbindelse er ekstremt ustabil og eksisterer kun i spormængder.
4. krypton tetrafluoroborate (KRBF4) :Denne forbindelse dannes ved at reagere KRF2 med bortrifluorid (BF3).
5. krypton tetraoxotetrafluorid (KRO4F4) :Denne forbindelse dannes ved at reagere KRF2 med iltdifluorid (OF2).
Det er vigtigt at bemærke, at de fleste af disse forbindelser er meget reaktive og ustabile, hvilket gør deres syntese og studerer udfordrende.
 Varme artikler
Varme artikler
-
 Rumtemperaturbundet grænseflade forbedrer afkøling af galliumnitrid-enhederTværsnit af lysfelt højopløsnings STEM-billeder af GaN-diamant-grænseflader bundet ved overfladeaktiveret bindingsteknik. Kredit:Zhe Cheng, Georgia Tech En rumtemperaturbindingsteknik til at integ
Rumtemperaturbundet grænseflade forbedrer afkøling af galliumnitrid-enhederTværsnit af lysfelt højopløsnings STEM-billeder af GaN-diamant-grænseflader bundet ved overfladeaktiveret bindingsteknik. Kredit:Zhe Cheng, Georgia Tech En rumtemperaturbindingsteknik til at integ -
 Mikrokapsler får en ny kraft - fjerner reaktive oxygenarterEugenia Kharlampieva, Veronika Kozlovskaya og Aaron Alford. Kredit:UAB Stabil, biokompatible mikrokapsler fra laboratoriet hos Eugenia Kharlampieva, Ph.D., har fået en ny kraft - evnen til at opfa
Mikrokapsler får en ny kraft - fjerner reaktive oxygenarterEugenia Kharlampieva, Veronika Kozlovskaya og Aaron Alford. Kredit:UAB Stabil, biokompatible mikrokapsler fra laboratoriet hos Eugenia Kharlampieva, Ph.D., har fået en ny kraft - evnen til at opfa -
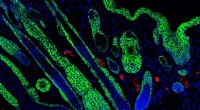 Sårhelende biomaterialer aktiverer immunsystemet for stærkere hudRegenererede hårsække i midten af et sår. Hårsækkene fremstår som dråbestrukturer, og de har Keratin 5 positive tips, som vises med grønt. Kredit:Tatiana Segura Lab, Duke University Forskere ved
Sårhelende biomaterialer aktiverer immunsystemet for stærkere hudRegenererede hårsække i midten af et sår. Hårsækkene fremstår som dråbestrukturer, og de har Keratin 5 positive tips, som vises med grønt. Kredit:Tatiana Segura Lab, Duke University Forskere ved -
 Samarbejde skaber et gennembrud for bæredygtig elektronikproduktionSFU Mechatronic Systems Engineering professor Woo Soo Kim samarbejder med schweiziske forskere om at udvikle en miljøvenlig 3D-printbar løsning til fremstilling af trådløse internet-of-Things-sensorer
Samarbejde skaber et gennembrud for bæredygtig elektronikproduktionSFU Mechatronic Systems Engineering professor Woo Soo Kim samarbejder med schweiziske forskere om at udvikle en miljøvenlig 3D-printbar løsning til fremstilling af trådløse internet-of-Things-sensorer


