2 Hvordan kan du forklare samhørighed og vedhæftning med hensyn til vandmolekyler?
samhørighed og vedhæftning i vandmolekyler:
samhørighed Henviser til tiltrækningen mellem molekyler af samme stof. I vand skyldes dette hydrogenbindingerne dannet mellem de lidt positive hydrogenatomer af et vandmolekyle og det lidt negative iltatom af et andet. Disse stærke bindinger holder vandmolekyler sammen, hvilket skaber en stærk overfladespænding, hvilket gør det muligt for ting som insekter at gå på vandet.
Adhæsion henviser til tiltrækningen mellem molekyler af forskellige stoffer. Vandmolekyler har en stærk affinitet for andre polære molekyler, som dem, der findes i glas eller træ. Dette skyldes igen den polære karakter af vandmolekylet og evnen til at danne brintbindinger med disse andre stoffer.
Her er en sammenbrud af, hvordan disse kræfter fungerer i hverdagens eksempler:
* samhørighed:
* overfladespænding: De stærke sammenhængende kræfter mellem vandmolekyler skaber en overfladespænding, der tillader genstande som en papirclip at flyde på vandet.
* Vanddråber: Tendensen til vandmolekyler til at klæbe sammen danner sfæriske dråber, hvilket minimerer deres overfladeareal på grund af samhørighed.
* Adhæsion:
* kapillær handling: Tiltrækningen mellem vandmolekyler og væggene i et smalt rør (som en plantes xylem) får vandet til at stige mod tyngdekraften på grund af vedhæftning og samhørighed, der arbejder sammen.
* befugtning: Vandmolekyler klæber let til polære overflader som glas, hvilket gør det "vådt". Dette står i kontrast til ikke-polære overflader som voks, der afviser vand.
Kortfattet:
* samhørighed: Vandmolekyler holder sig til hinanden på grund af stærke brintbindinger.
* Adhæsion: Vandmolekyler holder sig til andre polære stoffer, også på grund af dannelse af brintbinding.
Disse kræfter kombineret med de unikke egenskaber ved vand er vigtige for livet på jorden, letter processer som transport af næringsstoffer i planter, regulering af temperatur og understøttelse af akvatisk liv.
Sidste artikelEr komprimering af luft eller væske nyttigt?
Næste artikelHvad er krombicarbonat?
 Varme artikler
Varme artikler
-
 Fødevareforskere skaber sunde probiotiske drik fra sojapulpLektor Shao-Quan Liu og ph.d.-studerende Weng-Chan Vong fra NUS Food Science and Technology Program har udtænkt en unik cocktail af enzymer, probiotika og gær til at producere en okara-drik rig på tar
Fødevareforskere skaber sunde probiotiske drik fra sojapulpLektor Shao-Quan Liu og ph.d.-studerende Weng-Chan Vong fra NUS Food Science and Technology Program har udtænkt en unik cocktail af enzymer, probiotika og gær til at producere en okara-drik rig på tar -
 Mange små forskelle bidrager til en stor variationEt stof kan påvirke mennesker meget forskelligt. Kredit:Colourbox Der er ikke en enkelt hovedårsag til, at visse stoffer påvirker mennesker forskelligt, men derimod mange små faktorer. ETH-forsker
Mange små forskelle bidrager til en stor variationEt stof kan påvirke mennesker meget forskelligt. Kredit:Colourbox Der er ikke en enkelt hovedårsag til, at visse stoffer påvirker mennesker forskelligt, men derimod mange små faktorer. ETH-forsker -
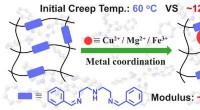 Metalkoordination muliggør høj temperatur, krybe-resistent polyimin vitrimer præparatLet forberedelse af polyimin vitrimere med forbedret krybebestandighed, termiske og mekaniske egenskaber via metalkoordination. Kredit:NIMTE Den biobaserede polymergruppe ved Ningbo Institute of M
Metalkoordination muliggør høj temperatur, krybe-resistent polyimin vitrimer præparatLet forberedelse af polyimin vitrimere med forbedret krybebestandighed, termiske og mekaniske egenskaber via metalkoordination. Kredit:NIMTE Den biobaserede polymergruppe ved Ningbo Institute of M -
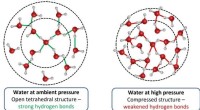 Kemikalier i celler fra marine organismer gør dem i stand til at overleve højtryk fundet i dybe oc…Denne grafik viser, hvordan det strukturelle netværk af vand forvrænges under højt tryk. Kredit:University of Leeds Forskere har opdaget, hvordan et kemikalie i cellerne i marine organismer gør dem
Kemikalier i celler fra marine organismer gør dem i stand til at overleve højtryk fundet i dybe oc…Denne grafik viser, hvordan det strukturelle netværk af vand forvrænges under højt tryk. Kredit:University of Leeds Forskere har opdaget, hvordan et kemikalie i cellerne i marine organismer gør dem
- Hvad kredserer Galaxy Orbit, hvis noget?
- Russisk søgemaskine advarer Google om mulige dataproblemer
- Kontrol af nanoclusters med overfladedefekter kan føre til konstruktion af nanoenheder (m/ video)
- Hvordan COVID-19 forbedrede vores forståelse af migration, medborgerskab og ulighed
- Forskere opdager nye måder at vride og skifte lys på
- Hvad er Fahrenheit for 36,5c?


