Hvad sker der med partikler i et stof, når det er opvarmet eller afkølet?
Opvarmning
* Øget kinetisk energi: Opvarmning af et stof giver energi til dets partikler, hvilket får dem til at vibrere og bevæge sig hurtigere. Dette kaldes en stigning i kinetisk energi.
* Større afstand: Når partikler bevæger sig hurtigere, kolliderer de oftere og med større kraft. Denne øgede bevægelse fører til en større gennemsnitlig afstand mellem partikler.
* statsændringer: Hvis der tilsættes nok varme, kan den øgede kinetiske energi overvinde kræfterne, der holder partikler sammen. Dette kan føre til en ændring af staten:
* fast til væske (smeltning): Partikler i et fast stof er tæt pakket og vibrerer i faste positioner. Opvarmning giver nok energi til at bryde disse bindinger, hvilket gør det muligt for partiklerne at bevæge sig mere frit, hvilket resulterer i en væske.
* væske til gas (kogning/fordampning): I en væske kan partikler bevæge sig mere frit, men tiltrækkes stadig af hinanden. Opvarmning gør det muligt for partikler at overvinde disse attraktioner og flygte ind i gasfasen.
afkøling
* Nedsat kinetisk energi: Afkøling fjerner energi fra partikler, hvilket får dem til at bremse og vibrere mindre. Dette er et fald i kinetisk energi.
* tættere afstand: Når partikler bevæger sig langsommere, kolliderer de sjældnere og med mindre kraft. Dette gør det muligt for de attraktive kræfter mellem partikler at trække dem tættere sammen.
* statsændringer: Fjernelse af nok varme kan få partiklerne til at bremse tilstrækkeligt til at ændre tilstand:
* gas til væske (kondens): Gaspartikler har en masse kinetisk energi og spredes langt fra hinanden. Køling bremser dem ned, hvilket giver attraktive kræfter mulighed for at trække dem nærmere og danne en væske.
* væske til fast (frysning): I en væske kan partikler bevæge sig mere frit. Afkøling får dem til at bremse og miste energi, hvilket får dem til at slå sig ned i et mere organiseret, fast arrangement i en solid tilstand.
Vigtige punkter:
* Temperatur: Temperaturen er et mål for den gennemsnitlige kinetiske energi af partiklerne i et stof.
* Specifik varmekapacitet: Forskellige stoffer kræver forskellige mængder varme for at ændre deres temperatur. Dette kaldes specifik varmekapacitet.
* udvidelse og sammentrækning: De fleste stoffer ekspanderer, når de opvarmes (partikler flytter længere fra hinanden) og sammentrækkes, når afkølet (partikler bevæger sig tættere sammen). Vand er en bemærkelsesværdig undtagelse, da det udvides, når det fryser.
Fortæl mig, hvis du gerne vil have mig til at uddybe ethvert specifikt punkt!
 Varme artikler
Varme artikler
-
 En rhodiumbaseret katalysator til fremstilling af organosilicium ved hjælp af mindre ædle metallerEt billede af hydrosilyleringsreaktionen ved anvendelse af den SiO2-understøttede katalysator bestående af et immobiliseret Rh-kompleks og tertiære aminer, med en omsætning på 260 (venstre) og nærmer
En rhodiumbaseret katalysator til fremstilling af organosilicium ved hjælp af mindre ædle metallerEt billede af hydrosilyleringsreaktionen ved anvendelse af den SiO2-understøttede katalysator bestående af et immobiliseret Rh-kompleks og tertiære aminer, med en omsætning på 260 (venstre) og nærmer -
 Hit-to-lead undersøgelser af en ny serie af små molekyle inhibitorer af DHODHKredit:CC0 Public Domain Enzymet dihydroorotate dehydrogenase (DHODH), en væsentlig komponent for de novo pyrimidin-ribonukleotid-biosyntese, er genopstået i de sidste par år som et mål for udvikl
Hit-to-lead undersøgelser af en ny serie af små molekyle inhibitorer af DHODHKredit:CC0 Public Domain Enzymet dihydroorotate dehydrogenase (DHODH), en væsentlig komponent for de novo pyrimidin-ribonukleotid-biosyntese, er genopstået i de sidste par år som et mål for udvikl -
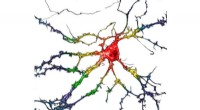 Forskere identificerer et psykedelisk lignende stof uden de hallucinogene bivirkningerEt repræsentativt billede af dyrkede dissocierede hippocampusneuroner, der midlertidigt udtrykker psychLight1 og psychLight2. Skala bar, 20 mm. Kredit:Calvin Ly Psykedeliske lægemidler har vist lø
Forskere identificerer et psykedelisk lignende stof uden de hallucinogene bivirkningerEt repræsentativt billede af dyrkede dissocierede hippocampusneuroner, der midlertidigt udtrykker psychLight1 og psychLight2. Skala bar, 20 mm. Kredit:Calvin Ly Psykedeliske lægemidler har vist lø -
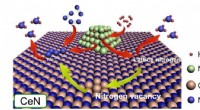 Fyldning af hulrummet i ammoniaksyntese:Nitrogenniveauernes rolle i katalysatorerNikkelpartikler dissocierer H2 for at tilvejebringe H -atomer til enten N -atomer fra selve CeN -krystalgitteret eller fremspringende N -atomer fra N2 -molekyler, der udfylder et nitrogenrum. I dette
Fyldning af hulrummet i ammoniaksyntese:Nitrogenniveauernes rolle i katalysatorerNikkelpartikler dissocierer H2 for at tilvejebringe H -atomer til enten N -atomer fra selve CeN -krystalgitteret eller fremspringende N -atomer fra N2 -molekyler, der udfylder et nitrogenrum. I dette
- 11 cm svarer til hvor mange inches?
- Når halvledere hænger sammen, materialer går kvante
- USA-bøde på Facebook sætter CEO Zuckerberg på krogen
- Røgsæsoner er ikke nye, men vores bestræbelser på at kontrollere skovbrande er, og burde ændre …
- Hvad er den molære masse af aluminiumnitrid?
- Hvad er Cheyne-Stokes Respiration?


