Hvor kan du finde en brintbinding?
Her er nogle steder, hvor du kan finde brintbindinger:
I biologiske systemer:
* Vand: Vandmolekyler holdes sammen af brintbindinger, hvilket giver vand sine unikke egenskaber som højt kogepunkt og overfladespænding.
* DNA og RNA: Hydrogenbindinger forbinder basisparene i DNA og RNA og holder den dobbelte helixstruktur sammen.
* Proteiner: Hydrogenbindinger hjælper med at stabilisere proteinstruktur og form, hvilket er afgørende for deres funktion.
* enzymer: Hydrogenbindinger bidrager til de specifikke interaktioner mellem enzymer og deres underlag, hvilket letter biokemiske reaktioner.
* Cellemembraner: Hydrogenbindinger spiller en rolle i strukturen og funktionen af cellemembraner.
i andre kemiske systemer:
* is: Hydrogenbindingerne i vandmolekyler er ansvarlige for den krystallinske struktur af is.
* flydende krystaller: Hydrogenbinding kan påvirke rækkefølge og egenskaber af flydende krystaller.
* polymerer: Hydrogenbindinger kan hjælpe med at holde polymerkæder sammen og påvirke deres egenskaber og opførsel.
* Organisk kemi: Hydrogenbinding kan forekomme mellem funktionelle grupper som alkoholer, aminer og amider.
I hverdagen:
* "klæbrighed" af våde overflader: Hydrogenbindingerne mellem vandmolekyler og overfladen er ansvarlige for de klæbende kræfter, vi føler.
* Evnen hos nogle materialer til at absorbere vand: Materialer som cellulose og bomuld kan absorbere vand på grund af hydrogenbinding mellem vandmolekyler og materialets molekyler.
Dette er ikke en udtømmende liste, men det giver dig en god idé om, hvor udbredt brintbinding er i naturen og forskellige systemer.
 Varme artikler
Varme artikler
-
 Nyt antibiotikum giver et slag mod bakteriel resistensEt farvet scanningselektronmikrografi af MRSA. Kredit:National Institute of Allergy and Infectious Diseases Forskere ved The Scripps Research Institute (TSRI) har givet nye superkræfter til et liv
Nyt antibiotikum giver et slag mod bakteriel resistensEt farvet scanningselektronmikrografi af MRSA. Kredit:National Institute of Allergy and Infectious Diseases Forskere ved The Scripps Research Institute (TSRI) har givet nye superkræfter til et liv -
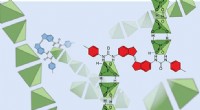 Skinner lys over den underlige verden af dihydrogenphosphatanionerRepræsentation, der viser dihydrogenphosphater (i grønt), der binder sammen i opløsning. Kredit:UNSW Forskere ved UNSW Sydney, sammen med samarbejdspartnere fra Western Sydney University og Hollan
Skinner lys over den underlige verden af dihydrogenphosphatanionerRepræsentation, der viser dihydrogenphosphater (i grønt), der binder sammen i opløsning. Kredit:UNSW Forskere ved UNSW Sydney, sammen med samarbejdspartnere fra Western Sydney University og Hollan -
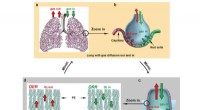 Et lunge-inspireret design gør vand til brændstofLighederne mellem udvekslingen af gasser i pattedyrs lunger og en nyudviklet mekanisme til at omdanne vand til brændstof. Kredit:Li et al . / Joule Forskere ved Stanford University har desig
Et lunge-inspireret design gør vand til brændstofLighederne mellem udvekslingen af gasser i pattedyrs lunger og en nyudviklet mekanisme til at omdanne vand til brændstof. Kredit:Li et al . / Joule Forskere ved Stanford University har desig -
 Efter madlavning, bioberigede majs og æg bevarer de nødvendige næringsstoffer for at forhindre bl…Kredit:American Chemical Society Berigede og bioberigede fødevarer er på forkant med indsatsen for at bekæmpe A-vitaminmangel på verdensplan. Men lidt er kendt om, hvilken indflydelse forarbejdnin
Efter madlavning, bioberigede majs og æg bevarer de nødvendige næringsstoffer for at forhindre bl…Kredit:American Chemical Society Berigede og bioberigede fødevarer er på forkant med indsatsen for at bekæmpe A-vitaminmangel på verdensplan. Men lidt er kendt om, hvilken indflydelse forarbejdnin


