Er det næsten umuligt at komprimere væsker og faste stoffer?
væsker:
* Kompressibilitet: Væsker er meget mindre komprimerbare end gasser, hvilket betyder, at de modstår ændringer i volumen under tryk. Dette skyldes, at deres molekyler er pakket meget tættere sammen.
* Praktisk kompressibilitet: Selvom det er meget svært at komprimere markant, oplever væsker en vis komprimering under ekstremt tryk. For eksempel lægger det dybe hav et enormt pres på vand, hvilket forårsager en lille reduktion i volumen.
* applikationer: Den lette kompressibilitet af væsker bruges i hydrauliske systemer, hvor trykket overføres gennem en væske for at udøve kraft.
faste stoffer:
* Kompressibilitet: Faststoffer er endnu mindre komprimerbare end væsker. Deres molekyler er tæt pakket i en stiv struktur og giver endnu stærkere modstand mod komprimering.
* Elasticitet: Faststoffer kan deformere under stress, men de har en tendens til at vende tilbage til deres oprindelige form, når stresset fjernes. Dette kaldes elasticitet, ikke komprimerbarhed.
* Undtagelser: Nogle materialer, som gummi, er mere komprimerbare end andre. Dette skyldes, at deres molekylære struktur giver mulighed for mere bevægelse under pres.
Key Takeaway:
Mens både væsker og faste stoffer betragtes som næsten ukomprimerbart I hverdagssituationer er det vigtigt at huske, at ekstreme pres kan forårsage en vis komprimering . Derudover adskiller udtrykket "kompressibilitet" sig fra "elasticitet", som henviser til evnen til at deformere og vende tilbage til den originale form.
Sidste artikelHvad er nogle eksempler på korrosion?
Næste artikelEr vand kendt som det universelle opløsningsmiddel?
 Varme artikler
Varme artikler
-
 Vurdering af begyndelsen af calciumphosphatkernen ved hyperpolariseret real-time NMRFor at skabe effektive funktionelle materialer, naturen tilbyder de bedste opskrifter ved at levere evolutionært vellykkede koncepter, siger Dennis Kurzbach fra Institut for Biologisk Kemi. Kredit:© S
Vurdering af begyndelsen af calciumphosphatkernen ved hyperpolariseret real-time NMRFor at skabe effektive funktionelle materialer, naturen tilbyder de bedste opskrifter ved at levere evolutionært vellykkede koncepter, siger Dennis Kurzbach fra Institut for Biologisk Kemi. Kredit:© S -
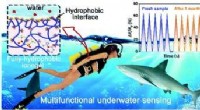 Fuldt hydrofob ionogel udviklet til bærbar undervandssensor og kommunikatorGrafisk abstrakt. Kredit:DOI:10.1039/D1MH00998B Smart Polymer Materials-gruppen ledet af professor Chen Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kinesiske
Fuldt hydrofob ionogel udviklet til bærbar undervandssensor og kommunikatorGrafisk abstrakt. Kredit:DOI:10.1039/D1MH00998B Smart Polymer Materials-gruppen ledet af professor Chen Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kinesiske -
 Forskning nulstilling på elektronisk næse til overvågning af luftkvalitet, diagnosticering af syg…Afbildning af et gassensorarray sammensat af mikroskalabalancer belagt med tynde film af nanoporøse materialer kaldet metalorganiske rammer. Kredit:Arni Sturluson, Melanie Huynh, OSU Ingeniørhøjskole
Forskning nulstilling på elektronisk næse til overvågning af luftkvalitet, diagnosticering af syg…Afbildning af et gassensorarray sammensat af mikroskalabalancer belagt med tynde film af nanoporøse materialer kaldet metalorganiske rammer. Kredit:Arni Sturluson, Melanie Huynh, OSU Ingeniørhøjskole -
 Forskere producerer første gang nogensinde videoer af kemisk syntese ved atomopløsningElektronmikroskopbilleder af testprøven ved forskellige forstørrelser. Kredit:(c) 2019 Nakamura et al. For første gang, forskere har formået at se tidligere utilgængelige detaljer om visse kemiske
Forskere producerer første gang nogensinde videoer af kemisk syntese ved atomopløsningElektronmikroskopbilleder af testprøven ved forskellige forstørrelser. Kredit:(c) 2019 Nakamura et al. For første gang, forskere har formået at se tidligere utilgængelige detaljer om visse kemiske
- Hvad er en kropsdel styret af Stenbukken i astronomi?
- Hurtigere opladning med diamanter
- Madaromaundersøgelse kan hjælpe med at forklare, hvorfor måltider smager dårligt i rummet
- Fysikere kvantesimulerer topologiske materialer med ultrakolde atomer
- Hvordan påvirker temperaturen lynet?
- NASA ser eks-Tropical Cyclone Debbie over Queensland


