Hvordan kan et atom, der har syv valenselektroner, fuldføre sit yderste niveau?
Her er hvorfor:
* octet regel: Atomer har en tendens til at være mest stabile, når de har otte elektroner i deres yderste skal (bortset fra brint og helium, som er stabile med to elektroner).
* Elektronegativitet: Atomer med syv valenselektroner er meget elektronegative, hvilket betyder, at de har en stærk attraktion for elektroner.
* ionisk binding: Ved at få en elektron opnår atomet en fuld ydre skal og bliver en negativt ladet ion (anion). Dette forekommer ofte gennem ionisk binding, hvor atomet danner et binding med et andet atom, der let mister et elektron (som et metal).
Eksempel:
Et kloratom (CL) har syv valenselektroner. Det kan få et elektron til at blive en chloridion (CL-), der har en komplet ydre skal af otte elektroner. Dette er grunden til, at klor ofte danner ioniske bindinger med metaller som natrium (NA) til dannelse af natriumchlorid (NaCl), almindeligvis kendt som bordsalt.
 Varme artikler
Varme artikler
-
 Proteiner daterer sig tilbage til sabeltandets tidKredit:University of Western Australia Planteforskere ved University of Western Australia har opdaget en helt ny familie af små proteiner kaldet PLPer (PawL Peptides), der dannes ved at piggybacke
Proteiner daterer sig tilbage til sabeltandets tidKredit:University of Western Australia Planteforskere ved University of Western Australia har opdaget en helt ny familie af små proteiner kaldet PLPer (PawL Peptides), der dannes ved at piggybacke -
 Materialer til medicinske kjoler gennemgår strenge testsTony Vindell udfører en af vandtestene på en stofprøve. Kredit:John Eisele Mens COVID-19-pandemien fortsætter med at fylde hospitaler rundt om i staten, flere Colorado-producenter håber på at sk
Materialer til medicinske kjoler gennemgår strenge testsTony Vindell udfører en af vandtestene på en stofprøve. Kredit:John Eisele Mens COVID-19-pandemien fortsætter med at fylde hospitaler rundt om i staten, flere Colorado-producenter håber på at sk -
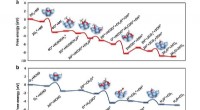 Ny zeolitter-sølvkatalysator booster formaldehydoxidation ved lave temperaturerFrienergidiagrammer over oxidationsprocesserne. a MF (rød linje) og b HCHO (blå linje) oxidation på henholdsvis Ag(100) overflade. Overgangstilstandsstrukturerne er vist som indskud, hvor Ag, C, O og
Ny zeolitter-sølvkatalysator booster formaldehydoxidation ved lave temperaturerFrienergidiagrammer over oxidationsprocesserne. a MF (rød linje) og b HCHO (blå linje) oxidation på henholdsvis Ag(100) overflade. Overgangstilstandsstrukturerne er vist som indskud, hvor Ag, C, O og -
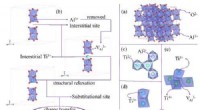 Forskere opdager oprindelsen af næsten ultraviolette og synlige absorptionsegenskaber af Ti:safir…Fig. 1. (a) Supercellestrukturen af Al2O3, (b) det mellemliggende Ti 3 + , Al ledig og substituerende Ti 3 + modeller, og deres transformationsproces, (c) linjekontakten Ti 3 + -Ti 3
Forskere opdager oprindelsen af næsten ultraviolette og synlige absorptionsegenskaber af Ti:safir…Fig. 1. (a) Supercellestrukturen af Al2O3, (b) det mellemliggende Ti 3 + , Al ledig og substituerende Ti 3 + modeller, og deres transformationsproces, (c) linjekontakten Ti 3 + -Ti 3
- Hvad er hastigheden på et plan, der bevæger sig med hastighed 450 km / h med vind r mph?
- Gigantisk jet spioneret fra sort hul i det tidlige univers
- Termonukleare flammer:Astrofysikere bruger supercomputer til at udforske eksotiske stjernefænomener…
- Syntetisk træ forbedrer soldampgenerering til høst af drikkevand
- Hvad er breddegrad og længdegrad i det sydlige kors?
- Et nærmere kig på antibiotikaresistente gener i luften


