Hvilken type krystallinsk fast stof er N2?
Her er hvorfor:
* molekylære faste stoffer dannes af tiltrækningen mellem molekyler. Disse attraktioner er relativt svage, såsom van der Waals -styrker.
* Nitrogen findes som diatomiske molekyler (N₂) holdt sammen af stærke kovalente bindinger i molekylet.
* Disse N₂ -molekyler interagerer med hinanden gennem svage London -spredningskræfter, som er ansvarlige for dens faste tilstand ved lave temperaturer.
Andre typer krystallinske faste stoffer:
* ioniske faste stoffer dannes af elektrostatiske attraktioner mellem modsat ladede ioner.
* Metalliske faste stoffer dannes af metalliske bindinger, hvor elektroner delokaliseres i hele det faste stof.
* kovalente netværksstoffer dannes af kovalente bindinger, der strækker sig gennem hele strukturen.
Da nitrogen ikke danner ioner eller har delokaliserede elektroner, passer det ikke ind i kategorierne af ioniske, metalliske eller kovalente netværksstoffer.
Sidste artikelHvad er N2 Plus H2-NH3 Blanced?
Næste artikelHvordan kan du afbalancere NH4NO2 giver n2 H2O?
 Varme artikler
Varme artikler
-
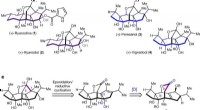 Kemikere syntetiserer perseanol for første gangen, Kemisk struktur, kulstofnummerering og ringsystembogstav tildeling for ryanodane (a) og isoryanodane (b) diterpener. c, Retrosyntetisk analyse af isoryanodane diterpen (+)-perseanol. [O], oxidatio
Kemikere syntetiserer perseanol for første gangen, Kemisk struktur, kulstofnummerering og ringsystembogstav tildeling for ryanodane (a) og isoryanodane (b) diterpener. c, Retrosyntetisk analyse af isoryanodane diterpen (+)-perseanol. [O], oxidatio -
 Forskere udvikler bioniske blade til distribueret landbrugKelsey Sakimoto, postdoc ved Center for Miljø, udforsker, hvordan man bruger solen til at berige jorden med et kunstigt blad og konstruerede bakterier. Kredit:Rose Lincoln/Harvard Staff Photographer
Forskere udvikler bioniske blade til distribueret landbrugKelsey Sakimoto, postdoc ved Center for Miljø, udforsker, hvordan man bruger solen til at berige jorden med et kunstigt blad og konstruerede bakterier. Kredit:Rose Lincoln/Harvard Staff Photographer -
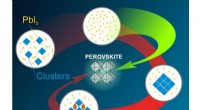 Kemikere bestemmer, hvordan man undgår biprodukter i syntesen af perovskitterRUDN -kemikere fandt ud af, hvordan man undgår biprodukter i syntesen af Perovskites Kredit:Natalia Deryugina En RUDN -professor, sammen med sine kolleger fra andre universiteter i Moskva, har b
Kemikere bestemmer, hvordan man undgår biprodukter i syntesen af perovskitterRUDN -kemikere fandt ud af, hvordan man undgår biprodukter i syntesen af Perovskites Kredit:Natalia Deryugina En RUDN -professor, sammen med sine kolleger fra andre universiteter i Moskva, har b -
 Lyser på, hvorfor plastik bliver gultKredit:ACS Applied Polymer Materials (2022). DOI:10.1021/acsapm.2c00877 Hvis du ejer en retro spillekonsol eller har en gammel rulle indpakningstape, har du set, hvordan plast bliver gult, når det
Lyser på, hvorfor plastik bliver gultKredit:ACS Applied Polymer Materials (2022). DOI:10.1021/acsapm.2c00877 Hvis du ejer en retro spillekonsol eller har en gammel rulle indpakningstape, har du set, hvordan plast bliver gult, når det
- Opbevarer en forbindelse ikke altid egenskaberne ved substaner, der udgør det?
- Hvordan kan stigninger i kuldioxid i luften påvirke verdens temperaturer?
- Fysiske egenskaber ved Styrofoam
- Anti-sommerfugleeffekt muliggør ny benchmarking af kvantecomputerens ydeevne
- Kosmiske magnetfelter med forbløffende orden
- Forskere genbruger beskadigede optiske polymerfibre til præcist at måle magnetiske felter


