Hvorfor faste stoffer er bedre varmeledere end gasser?
1. Partikelafstand:
* faste stoffer: Partikler i faste stoffer er tæt pakket sammen med meget lidt plads mellem dem.
* Gasser: Partikler i gasser er vidt adskilt og bevæger sig frit.
2. Partikelinteraktioner:
* faste stoffer: Den nærhed af partikler i faste stoffer fører til stærke intermolekylære kræfter, såsom ioniske bindinger, metalliske bindinger eller kovalente bindinger. Disse kræfter begrænser partikelbevægelsen og giver mulighed for effektiv energioverførsel.
* Gasser: De svage intermolekylære kræfter i gasser gør det muligt for partikler at bevæge sig frit og kolliderer sjældnere.
3. Energioverførselsmekanismer:
* faste stoffer: Varmeoverførsel i faste stoffer forekommer primært gennem ledning , hvor vibrerende atomer overfører energi til deres naboer gennem kollisioner. Partiklernes nærhed letter effektiv energioverførsel gennem denne mekanisme.
* Gasser: Varmeoverførsel i gasser er hovedsageligt gennem konvektion , hvor varmere, mindre tætte gasstigninger og køligere, tættere gas dræner. Denne proces er mindre effektiv end ledning på grund af den større afstand mellem partikler og svagere interaktioner.
Kortfattet:
* faste stoffer: Stram pakning og stærke interaktioner muliggør effektiv energioverførsel gennem ledning.
* Gasser: Bred afstand og svage interaktioner hindrer energioverførsel, hvilket gør dem til dårlige ledere af varme.
Derfor er faste stoffer generelt bedre varmeledere end gasser.
 Varme artikler
Varme artikler
-
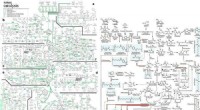 Et omfattende metabolisk kort til produktion af biobaserede kemikalierBiobaseret kemikalieproduktion ad biologiske og kemiske veje. Dette metaboliske kort beskriver repræsentative kemikalier, der kan fremstilles enten ved biologiske og/eller kemiske midler. Røde pile re
Et omfattende metabolisk kort til produktion af biobaserede kemikalierBiobaseret kemikalieproduktion ad biologiske og kemiske veje. Dette metaboliske kort beskriver repræsentative kemikalier, der kan fremstilles enten ved biologiske og/eller kemiske midler. Røde pile re -
 Farveændrende kontaktlinse kan forbedre overvågningen af behandlinger med øjensygdommeKontaktlinser, der skifter farve efter at have frigivet lægemidler i øjet, kan hjælpe læger med at afgøre, om en medicin bliver leveret til det tilsigtede behandlingssted. Kredit:American Chemical Soc
Farveændrende kontaktlinse kan forbedre overvågningen af behandlinger med øjensygdommeKontaktlinser, der skifter farve efter at have frigivet lægemidler i øjet, kan hjælpe læger med at afgøre, om en medicin bliver leveret til det tilsigtede behandlingssted. Kredit:American Chemical Soc -
 Hvad skal vi gøre ved engangsplast?Kredit:Ames Laboratory Meget af den voksende globale bekymring for plasten, der forurener vores oceaner og tilstopper vores lossepladser, har fokuseret på at reducere forbruget og genbruge, hvor v
Hvad skal vi gøre ved engangsplast?Kredit:Ames Laboratory Meget af den voksende globale bekymring for plasten, der forurener vores oceaner og tilstopper vores lossepladser, har fokuseret på at reducere forbruget og genbruge, hvor v -
 Et nærmere kig på tredjehåndsrygning og dens risiciVed at bruge state-of-the-art teknikker har forskere opnået en bedre forståelse af den komplekse blanding af farlige kemikalier i tredjehåndsrygning - den resterende forurening fra cigaretrygning - so
Et nærmere kig på tredjehåndsrygning og dens risiciVed at bruge state-of-the-art teknikker har forskere opnået en bedre forståelse af den komplekse blanding af farlige kemikalier i tredjehåndsrygning - den resterende forurening fra cigaretrygning - so
- Vrede, da jernbanebyggeriet begynder i Nairobi National Park
- Hvad sker der ved den bevægelige kant af en revne?
- Kældermembranlaget af huden adskiller hvad?
- Olie- og gasefterforskning og -produktion truer store ørkenflodsystemer
- Suomi NPP-satellitvisninger New South Wales-brande raser videre
- Hvor mange liter i 35 ounces?


