Hvad er forskellen mellem elektronegativitet af kulstof og svovl?
Dette betyder, at svovl er lidt mere elektronegativ end kulstof, men forskellen er meget lille.
Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner i en binding. Jo højere elektronegativitet, jo stærkere er det stærkere.
Mens forskellen mellem kulstof og svovl er let, kan den stadig påvirke egenskaberne ved molekyler, der indeholder disse elementer. For eksempel i carbondisulfid (CS₂) er svovlatomerne lidt mere elektronegative, hvilket fører til en polær binding. Denne polaritet påvirker molekylets samlede egenskaber, såsom dets kogepunkt og opløselighed.
 Varme artikler
Varme artikler
-
 At finde træalternativer til truet ibenholtEn violin med et gribebræt lavet af schweizisk ibenholt. Kredit:Wilhelm Geigenbau AG, Suhr Ligesom mange tropiske træsorter, ibenholt er en truet art, der er vanskelig at bruge, sådan i instrument
At finde træalternativer til truet ibenholtEn violin med et gribebræt lavet af schweizisk ibenholt. Kredit:Wilhelm Geigenbau AG, Suhr Ligesom mange tropiske træsorter, ibenholt er en truet art, der er vanskelig at bruge, sådan i instrument -
 Et bannerår for pharmaKredit:CC0 Public Domain Da 2018 lakker mod enden, medicinalindustrien fejrer et fremgangsår med nye investeringer og terapeutiske gennembrud. Disse succeser var drevet af banebrydende videnskab o
Et bannerår for pharmaKredit:CC0 Public Domain Da 2018 lakker mod enden, medicinalindustrien fejrer et fremgangsår med nye investeringer og terapeutiske gennembrud. Disse succeser var drevet af banebrydende videnskab o -
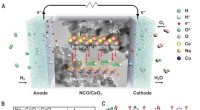 Reduktion af driftstemperaturen for keramiske brændselsceller med en elektrolyt med høj protonledn…Design af NCO/CeO2-heterostrukturfunktionerne til hurtig protonmigrering. Kredit: Videnskab (2020). DOI:10.1126/science.aaz9139 Et team af forskere tilknyttet flere institutioner i Kina har udvik
Reduktion af driftstemperaturen for keramiske brændselsceller med en elektrolyt med høj protonledn…Design af NCO/CeO2-heterostrukturfunktionerne til hurtig protonmigrering. Kredit: Videnskab (2020). DOI:10.1126/science.aaz9139 Et team af forskere tilknyttet flere institutioner i Kina har udvik -
 Kumarinforbindelser fra egetræsfade kunne bidrage til bitter smag i vin og spiritusKredit:Pixabay/CC0 Public Domain Vin og spiritus er komplekse blandinger af smags- og aromaforbindelser, hvoraf nogle opstår under lagring i træfade. Blandt andre forbindelser, egetræ frigiver kum
Kumarinforbindelser fra egetræsfade kunne bidrage til bitter smag i vin og spiritusKredit:Pixabay/CC0 Public Domain Vin og spiritus er komplekse blandinger af smags- og aromaforbindelser, hvoraf nogle opstår under lagring i træfade. Blandt andre forbindelser, egetræ frigiver kum
- Hvilken lys stjerne vises i øst om natten sydafrikansk himmel?
- Hvad har dyreceller ikke den plante ikke?
- Nye NASA-billeder viser massiv raketeksplosion i Virginia
- En ny film, der fordamper sved seks gange hurtigere og holder 15 gange mere fugt
- Hvilken idé om baseret på fossiler og de moderne organismer, han fandt, siger dybest set, at genet…
- Hvis du vælter fra din træhytte konstant får fart, når du falder til jorden under t, overtræder…


