Hvad er den vigtigste rolle ved hydrogenbinding mellem vandmolekyler?
* Højt kogepunkt: Hydrogenbindinger kræver en betydelig mængde energi at bryde, hvilket resulterer i, at vand har et meget højere kogepunkt end forventet for et molekyle af dens størrelse. Dette gør det muligt for vand at eksistere som en væske over en lang række temperaturer, afgørende for livet.
* højt smeltepunkt: Af samme grund som ovenfor har vand et relativt højt smeltepunkt. Dette betyder, at vand forbliver flydende over en bred vifte af temperaturer, igen afgørende for livet.
* Høj specifik varmekapacitet: Vand kan absorbere en masse varme, før dens temperatur øges markant. Dette gør vand til en fremragende temperaturregulator, både i miljøet og inden for levende organismer.
* høj fordampningsvarme: Der kræves en betydelig mængde varme for at omdanne vand fra en væske til en gas (fordampning). Dette gør svedt til en effektiv kølemekanisme for dyr.
* opløsningsmiddelegenskaber: Vands polaritet og evne til at danne hydrogenbindinger gør det til et fremragende opløsningsmiddel for mange stoffer, hvilket muliggør transport af næringsstoffer og affaldsprodukter i levende organismer.
* overfladespænding: Hydrogenbindinger skaber en stærk sammenhængende kraft mellem vandmolekyler, hvilket fører til høj overfladespænding. Dette giver insekter mulighed for at gå på vand og hjælper med vandtransport i planter.
Sammenfattende er hydrogenbinding ansvarlig for en række egenskaber, der gør vand til det universelle opløsningsmiddel og gør livet på jorden muligt.
 Varme artikler
Varme artikler
-
 Lys og peptider:Ny metode diversificerer livets naturlige byggestenSollys eksperiment. Reaktionerne kan udføres ved hjælp af lyset fra solen i en enkel glaskolbe. Kredit:J. Waser/EPFL Opdagelse af nye biologiske mål er en kritisk del af vores igangværende kamp mo
Lys og peptider:Ny metode diversificerer livets naturlige byggestenSollys eksperiment. Reaktionerne kan udføres ved hjælp af lyset fra solen i en enkel glaskolbe. Kredit:J. Waser/EPFL Opdagelse af nye biologiske mål er en kritisk del af vores igangværende kamp mo -
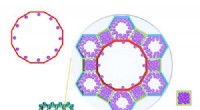 Realtidsanalyse af MOF-adsorptionsadfærdSkematisk illustration af molekyler adsorberet på metalorganiske rammer med forskellige porer af forskellige strukturer, hvor In-situ røntgenkrystallografi er blevet udviklet til at klassificere hver
Realtidsanalyse af MOF-adsorptionsadfærdSkematisk illustration af molekyler adsorberet på metalorganiske rammer med forskellige porer af forskellige strukturer, hvor In-situ røntgenkrystallografi er blevet udviklet til at klassificere hver -
 Fremstilling af åbne mesoporøse carbon nanofibre til fleksible og bærbare strømkilderKredit:CC0 Public Domain Med den nyligt stigende udvikling af letvægts, transportabel, fleksibel og bærbar elektronik til sundheds- og biomedicinsk udstyr, der er et presserende behov for at udfor
Fremstilling af åbne mesoporøse carbon nanofibre til fleksible og bærbare strømkilderKredit:CC0 Public Domain Med den nyligt stigende udvikling af letvægts, transportabel, fleksibel og bærbar elektronik til sundheds- og biomedicinsk udstyr, der er et presserende behov for at udfor -
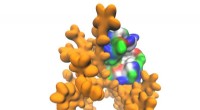 Forskere skaber multifunktionelle protein-polymerfilmDendrimer-molekyle er markeret gult. Overfladen af proteinmolekylet er farvekodet i overensstemmelse med de kemiske egenskaber af aminosyrerester (rød - positiv ladning, blå -- negativ ladning, grøn
Forskere skaber multifunktionelle protein-polymerfilmDendrimer-molekyle er markeret gult. Overfladen af proteinmolekylet er farvekodet i overensstemmelse med de kemiske egenskaber af aminosyrerester (rød - positiv ladning, blå -- negativ ladning, grøn
- Officiel:Kinas månesonde vil bære fransk, russisk gear
- Wearables kan få boost fra borinfunderet grafen
- LISA:Registrering af eksoplaneter ved hjælp af gravitationsbølger
- Hvilken faktor ville sandsynligvis forstyrre genetisk ligevægt i en stor population?
- Sammenlignet med lysstyrken og overfladetemperaturen for rød hovedsekvens er starsbue supergiants?
- Farveændringstest for at hjælpe kræftforskningen videre


