Et heliumatom har 2 elektroner i sit første og eneste energiniveau. Ville du forudsige, at let danner forbindelser med andre elementer?
* stabil elektronkonfiguration: Helium har en fuld ydre skal (dets eneste energiniveau) med to elektroner. Dette er en meget stabil konfiguration, der ligner de ædle gasser. Atomer stræber efter stabilitet, og helium har det allerede.
* Høj ioniseringsenergi: Det kræver en masse energi at fjerne et elektron fra helium på grund af dets stabile konfiguration. Dette gør det usandsynligt at miste en elektron og danne en positiv ion.
* Lav elektronegativitet: Helium har en meget lav elektronegativitet, hvilket betyder, at den har en meget svag attraktion for elektroner. Dette gør det usandsynligt at vinde elektroner og danne en negativ ion.
Kortfattet: Heliums stabile elektronkonfiguration, høj ioniseringsenergi og lav elektronegativitet gør det meget ureaktivt. Det er så ureaktivt, at det sjældent danner forbindelser med andre elementer.
 Varme artikler
Varme artikler
-
 Det er ikke vibranium eller proto-adamantium, men forskeres nye legering kommer tæt påKredit:University of North Texas Fire gange stærkere end rustfrit stål, en unik legering blander krom, kobolt, jern, mangan og silicium. Det er ikke Black Panthers vibranium eller Captain America
Det er ikke vibranium eller proto-adamantium, men forskeres nye legering kommer tæt påKredit:University of North Texas Fire gange stærkere end rustfrit stål, en unik legering blander krom, kobolt, jern, mangan og silicium. Det er ikke Black Panthers vibranium eller Captain America -
 Kemiker viser, at intermolekylære interaktioner kan opnå hidtil ukendte dimensionerKredit:The Journal of Physical Chemistry Letters Intermolekylære interaktioner er de kræfter, der vedrører molekyler. Generelt strækker disse interaktioner sig næppe ud over molekylernes grænser.
Kemiker viser, at intermolekylære interaktioner kan opnå hidtil ukendte dimensionerKredit:The Journal of Physical Chemistry Letters Intermolekylære interaktioner er de kræfter, der vedrører molekyler. Generelt strækker disse interaktioner sig næppe ud over molekylernes grænser. -
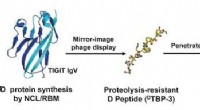 Checkpoint blokade af et D-peptid til cancer immunterapiKredit:Angewandte Chemie Vores immunsystem burde være i stand til at genkende og dræbe tumorceller. Imidlertid, mange tumorer bedrager immunsystemet. For eksempel, de inducerer T-cellers såkaldte
Checkpoint blokade af et D-peptid til cancer immunterapiKredit:Angewandte Chemie Vores immunsystem burde være i stand til at genkende og dræbe tumorceller. Imidlertid, mange tumorer bedrager immunsystemet. For eksempel, de inducerer T-cellers såkaldte -
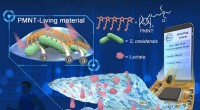 Fleksibel bioelektronisk enhed baseret på levende materiale til overvågning af laktat- og tumorcel…Skematisk diagram af PMNT-baseret levende materiale og bioelektronisk enhed til overvågning af laktat i fysiologiske væsker (sved, urin og plasma) og tælling af tumorceller. Kredit:Wang Zenghao Eft
Fleksibel bioelektronisk enhed baseret på levende materiale til overvågning af laktat- og tumorcel…Skematisk diagram af PMNT-baseret levende materiale og bioelektronisk enhed til overvågning af laktat i fysiologiske væsker (sved, urin og plasma) og tælling af tumorceller. Kredit:Wang Zenghao Eft
- Kameraet fanger innovativ træksejlads i rummet
- Grumman EA-6B Prowler
- Hvorfor valgte du mRNA snarere end genomisk DNA til at fremstille et bibliotek?
- Hvordan digital religion former spiritualitet blandt millennials
- Hvordan var klimaet i Yanomamo?
- Multidimensionel kohærent spektroskopi afslører triplet tilstandssammenhænge i cæsium bly-haloge…


