Forklar, hvorfor destillation er en god måde at adskille væsker i C8H18 og C5H12?
Her er hvorfor:
* Kogepunktforskel: Octane har et højere kogepunkt (125,7 ° C) sammenlignet med pentan (36,1 ° C). Denne forskel i kogepunkter er betydelig, hvilket gør dem let adskillelige ved destillation.
* destillationsproces: Ved destillation opvarmes blandingen. Komponenten med det lavere kogepunkt (pentan) fordamper først, hvilket efterlader den højere kogepunktkomponent (octane) bag sig.
* dampsamling: Pentandampen opsamles og kondenseres tilbage i flydende form, hvilket resulterer i en ren pentanprøve. Den resterende væske i destillationskolben er primært oktan.
Her er en forenklet sammenbrud:
1. Opvarmning: Blandingen af oktan og pentan opvarmes.
2. fordampning: Pentan, med sit lavere kogepunkt, fordamper først.
3. Kondens: Pentandampen afkøles og kondenseres tilbage i flydende form og adskiller den fra oktanen.
4. samling: Den rene pentanvæske opsamles separat.
5. Resterende oktan: Væsken, der er tilbage i destillationskolben, er primært oktan.
Derfor giver den signifikante forskel i kogepunkter mellem oktan og pentan mulighed for effektiv adskillelse ved hjælp af destillation.
 Varme artikler
Varme artikler
-
 Udvikling af bæredygtige membraner til fremtidig energiDr. Suzana Nunes (til venstre), KAUST-professor i kemi- og miljøvidenskab og teknik, og Dr. Stefan Chisca (til højre), KAUST-forsker, undersøger en beholder med polymeren, der bruges til at fremstille
Udvikling af bæredygtige membraner til fremtidig energiDr. Suzana Nunes (til venstre), KAUST-professor i kemi- og miljøvidenskab og teknik, og Dr. Stefan Chisca (til højre), KAUST-forsker, undersøger en beholder med polymeren, der bruges til at fremstille -
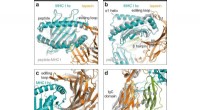 Molekylære chaperoninteraktioner visualiseret gennem røntgenstrukturanalyseKonformationelle ændringer ved klient-chaperone engagement. et topbillede af superpositionering af peptid-receptiv MHC I i chaperonkomplekset (MHC I hc, teal; tapasin, orange) med peptidbundet H2-Db (
Molekylære chaperoninteraktioner visualiseret gennem røntgenstrukturanalyseKonformationelle ændringer ved klient-chaperone engagement. et topbillede af superpositionering af peptid-receptiv MHC I i chaperonkomplekset (MHC I hc, teal; tapasin, orange) med peptidbundet H2-Db ( -
 Brug af elektricitet til at give kemi et løftUD-forskere har udviklet en ny metode til fremstilling af jernbaserede metalorganiske rammer (MOF) materialer. På billedet:Kandidatstuderende Amanda Weaver (til venstre) sætter gang i den UD-udviklede
Brug af elektricitet til at give kemi et løftUD-forskere har udviklet en ny metode til fremstilling af jernbaserede metalorganiske rammer (MOF) materialer. På billedet:Kandidatstuderende Amanda Weaver (til venstre) sætter gang i den UD-udviklede -
 Fremstilling af bæredygtige polymerer fra duftende molekylerKredit:CC0 Public Domain En måde at fremstille organiske polymerer på fra de duftende molekyler i nåletræer og frugttræer er blevet udviklet af forskere ved University of Birmingham. Teknikken, u
Fremstilling af bæredygtige polymerer fra duftende molekylerKredit:CC0 Public Domain En måde at fremstille organiske polymerer på fra de duftende molekyler i nåletræer og frugttræer er blevet udviklet af forskere ved University of Birmingham. Teknikken, u
- Hvad er de afstande, der er repræsenteret af et let år, en astronomisk enhed og parsec?
- Hvordan kan forskere teste deres ideer om universets oprindelse, hvis de fysisk interagerer med elle…
- Hvad er gråt metal?
- Undersøgelse:Mest sete tv-shows forenkler, stereotype problemer med hjemløshed
- Kan der høres en eksplosion på månens overflade?
- Syntetiske beklædningsfibre bidrager med store mængder plastikforurening på land


