Hvad er ikke-krystallinsk?
Her er en sammenbrud:
Krystallinske materialer:
* bestilt struktur: Atomer eller molekyler er arrangeret i et meget regelmæssigt, gentagne mønster.
* rækkefølge: Det gentagne mønster strækker sig over hele materialet.
* skarpt smeltepunkt: De smelter ved en bestemt temperatur.
* anisotropisk: Deres egenskaber kan variere i forskellige retninger.
* Eksempler: Diamanter, salt, kvarts
Ikke-krystallinske (amorfe) materialer:
* forstyrret struktur: Atomer eller molekyler er arrangeret tilfældigt.
* ordre på kort rækkevidde: Order findes kun over korte afstande.
* gradvis blødgøring: De blødgøres over en række temperaturer i stedet for at smelte kraftigt.
* isotropisk: Deres egenskaber er de samme i alle retninger.
* Eksempler: Glas, gummi, plast, honning
Nøgleegenskaber ved ikke-krystallinske materialer:
* Mangel på lang rækkevidde: Dette er det definerende træk ved ikke-krystallinske materialer.
* Højere entropi: De har en højere grad af forstyrrelse, hvilket fører til højere entropi sammenlignet med krystallinske materialer.
* Variable egenskaber: Deres egenskaber kan tilpasses ved at kontrollere graden af uorden.
* bred vifte af applikationer: De bruges i forskellige applikationer på grund af deres unikke egenskaber.
Eksempler på ikke-krystallinske materialer:
* glas: Fremstillet ved afkøling smeltet silica hurtigt, hvilket forhindrer krystallisation.
* polymerer: Lange kæder af molekyler kan arrangeres tilfældigt og skabe en amorf struktur.
* Metaller: Nogle metaller kan slukkes hurtigt fra en smeltet tilstand for at producere en ikke-krystallinsk struktur.
* væsker: De fleste væsker, som vand og olie, er ikke-krystallinske på grund af den tilfældige bevægelse af deres molekyler.
Kortfattet:
Ikke-krystallinske materialer er kendetegnet ved deres mangel på lang rækkevidde, hvilket fører til unikke egenskaber og applikationer sammenlignet med deres krystallinske kolleger.
 Varme artikler
Varme artikler
-
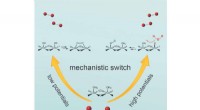 Potentialafhængig afbryder hjælper med vandopdeling ved hjælp af koboltoxid-katalysatorerEn potentialafhængig afbryder hjælper med vandspaltning ved hjælp af cobaltoxid-katalysatorer, Boston College og Yale University-forskere rapporterer i tidsskriftet Chem. Lille elektrisk ladning drive
Potentialafhængig afbryder hjælper med vandopdeling ved hjælp af koboltoxid-katalysatorerEn potentialafhængig afbryder hjælper med vandspaltning ved hjælp af cobaltoxid-katalysatorer, Boston College og Yale University-forskere rapporterer i tidsskriftet Chem. Lille elektrisk ladning drive -
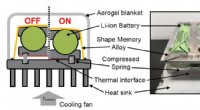 Termiske høreværn beskytter mobiltelefonens batterier mod ekstreme temperaturerDer vises en skematisk og foto af en termisk regulator designet af Berkeley-ingeniører til passivt at holde lithium-ion-batterier inden for et optimalt temperaturområde. Ved højere temperaturer, ledni
Termiske høreværn beskytter mobiltelefonens batterier mod ekstreme temperaturerDer vises en skematisk og foto af en termisk regulator designet af Berkeley-ingeniører til passivt at holde lithium-ion-batterier inden for et optimalt temperaturområde. Ved højere temperaturer, ledni -
 Plastfilm beskytter overflader mod ny coronavirus ved kontaktLaboratorietests viste, at film indeholdende sølv-silica nanopartikler var i stand til at fjerne 99,84% af SARS-CoV-2 partikler efter eksponering i to minutter. Kredit:Promaflex En klæbende plastf
Plastfilm beskytter overflader mod ny coronavirus ved kontaktLaboratorietests viste, at film indeholdende sølv-silica nanopartikler var i stand til at fjerne 99,84% af SARS-CoV-2 partikler efter eksponering i to minutter. Kredit:Promaflex En klæbende plastf -
 Konstrueret gær kunne udvide biobrændstoffers rækkeviddeKredit:CC0 Public Domain At øge produktionen af biobrændstoffer som ethanol kan være et vigtigt skridt i retning af at reducere det globale forbrug af fossile brændstoffer. Imidlertid, ethanolpr
Konstrueret gær kunne udvide biobrændstoffers rækkeviddeKredit:CC0 Public Domain At øge produktionen af biobrændstoffer som ethanol kan være et vigtigt skridt i retning af at reducere det globale forbrug af fossile brændstoffer. Imidlertid, ethanolpr
- Hvordan påvirker en øget masse af din beskyttende beholder tyngdekraften på beholderen?
- Hvordan patogene bakterier forbereder et klæbrigt adhæsionsprotein
- Hvad ville der ske, hvis kernen i solen findes?
- Sådan beregnes Antilog
- Forskere ser på naturen for at finde frem til hemmelighederne ved cyklisk imin -spaltning
- Sådan konverteres Hz til HP


