En geolog tester en klippe indeholdende calciumoxid ved at reagere det med saltsyre. Vand- og chloridform. Hvilke obligationer bryder?
reaktionen
Calciumoxid (CAO) reagerer med saltsyre (HCI) for at producere calciumchlorid (CaCl₂) og vand (H₂O).
Den afbalancerede kemiske ligning er:
Cao + 2 HCl → Cacl₂ + H₂O
obligationer Breaking
* ionisk binding i calciumoxid (CAO): Calciumoxidmolekylet holdes sammen af en ionisk binding. Calciumatomet (CA) mister to elektroner for at blive en positivt ladet ion (Ca²⁺), og iltatomet (O) får disse to elektroner til at blive en negativt ladet ion (O²⁻). De modsatte ladninger tiltrækker og danner den ioniske binding. Denne binding går i stykker, når calciumoxid reagerer med saltsyre.
* kovalent binding i saltsyre (HCL): Hydrochlorsyre består af et hydrogenatom (H) og et chloratom (CL) holdt sammen af en enkelt kovalent binding. I denne binding deler brint- og chloratomer et par elektroner. Denne binding går i stykker, når saltsyren reagerer med calciumoxid.
nye obligationer form
* ionisk binding i calciumchlorid (cacl₂): Calciumchlorid holdes også sammen af en ionisk binding. Calciumionen (Ca²⁺) danner nu ioniske bindinger med to chloridioner (CL⁻).
* kovalent binding i vand (H₂O): Vandmolekyler dannes med kovalente bindinger mellem to hydrogenatomer og et iltatom.
Kortfattet
Reaktionen involverer at bryde ioniske bindinger i calciumoxid og kovalente bindinger i saltsyre. Nye ioniske bindinger dannes i calciumchlorid, og nye kovalente bindinger dannes i vand.
Sidste artikelHvordan kommer et atom ion?
Næste artikelHvad er den eneste måde at bekræfte, at en kemisk ændring har fundet sted?
 Varme artikler
Varme artikler
-
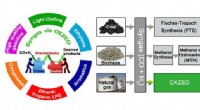 Oxid-zeolit-baseret komposit katalysator koncept muliggør syngas kemi ud over Fischer-Tropsch synte…Oxid-zeolit-baseret kompositkatalysatorkoncept, der muliggør syngaskemi ud over Fischer-Tropsch-syntese. Kredit:JIAO Feng og MIAO Dengyun Fischer-Tropsch-syntese (FTS) er blevet anvendt som kernet
Oxid-zeolit-baseret komposit katalysator koncept muliggør syngas kemi ud over Fischer-Tropsch synte…Oxid-zeolit-baseret kompositkatalysatorkoncept, der muliggør syngaskemi ud over Fischer-Tropsch-syntese. Kredit:JIAO Feng og MIAO Dengyun Fischer-Tropsch-syntese (FTS) er blevet anvendt som kernet -
 Røntgenbilleder giver fingerpeg om brud i solid-state batterierMatthew McDowell, en assisterende professor ved George W. Woodruff School of Mechanical Engineering og School of Materials Science and Engineering, undersøger batterier i en cykelstation. Kredit:Rob F
Røntgenbilleder giver fingerpeg om brud i solid-state batterierMatthew McDowell, en assisterende professor ved George W. Woodruff School of Mechanical Engineering og School of Materials Science and Engineering, undersøger batterier i en cykelstation. Kredit:Rob F -
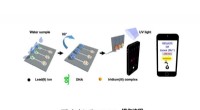 Ny enhed til hurtig og præcis detektering af blyDiagrammet viser detektionsprocessen. Kredit:HKBU Et forskerhold fra Institut for Kemi ved Hong Kong Baptist University (HKBU) har opfundet en bærbar enhed til one-stop-detektion af blykoncentrati
Ny enhed til hurtig og præcis detektering af blyDiagrammet viser detektionsprocessen. Kredit:HKBU Et forskerhold fra Institut for Kemi ved Hong Kong Baptist University (HKBU) har opfundet en bærbar enhed til one-stop-detektion af blykoncentrati -
 Forskere finder konformationsforstyrrelser, der indstiller ladningsbærermobilitet i 2-D perovskitte…Repræsentative transiente THz -transmissionsændringer, ΔT/T, af HA2PbI4 (n =6) for forskellige excitationsfluenser (λpump =400 nm). Symboler repræsenterer eksperimentelle data, mens faste linjer passe
Forskere finder konformationsforstyrrelser, der indstiller ladningsbærermobilitet i 2-D perovskitte…Repræsentative transiente THz -transmissionsændringer, ΔT/T, af HA2PbI4 (n =6) for forskellige excitationsfluenser (λpump =400 nm). Symboler repræsenterer eksperimentelle data, mens faste linjer passe
- Ved at udskille hormoner får Tymus, hvilke celler til at blive immunkompetente?
- Dødsraterne for sorte og hvide soldater i Koreakrigen var ens uanset adskillelse, undersøgelse fin…
- Sådan måles kulstofdannelse i læskedrikke til et videnskabsprojekt
- Hvilken tektonisk plade er nærmest Delaware?
- Hvad er 4,6 grader Celsius i Fahrenheit?
- Hvor lang tid ville det tage at bestige Vesuv?


