Hvad er formålet med mættet NaCl -opløsning til vask af et organisk lag Hvorfor ikke bruge deioniseret vand?
Hvorfor mættet NaCl -løsning?
* Salting ud: Den primære årsag til at bruge en mættet NaCl -løsning (også kendt som saltvand) er at fremme saltning . Dette fænomen er afhængig af princippet om, at salte (som NaCl) mindsker opløseligheden af organiske forbindelser i vand.
* Når du tilsætter saltvand til et vandigt lag indeholdende opløste organiske forbindelser, tvinger den øgede saltkoncentration de organiske forbindelser ud af den vandige fase og ind i den organiske fase. Dette gør adskillelsen af lagene mere effektiv.
* Reduktion af emulsioner: Brine hjælper også med at reducere dannelsen af emulsioner. Emulsioner er blandinger af to ikke -blandbare væsker (som vand og et organisk opløsningsmiddel), der danner en overskyet, ustabil blanding. Brats høje densitet hjælper med at adskille lagene lettere, hvilket gør det lettere at fjerne det vandige lag.
Hvorfor ikke bare deioniseret vand?
* Begrænset effektivitet: Mens deioniseret vand kan hjælpe med at vaske nogle urenheder væk fra det organiske lag, vil det ikke være så effektivt som saltlage til at fjerne opløste organiske forbindelser. Deioniseret vand "salt" de organiske forbindelser ikke så effektivt ud.
* Emulsionsdannelse: Deioniseret vand kan endda øge sandsynligheden for dannelse af emulsion, da den nedre tæthed af vand sammenlignet med det organiske lag kan føre til mere blanding og mindre klar adskillelse.
Kortfattet:
Brug af en mættet NaCl -opløsning til vask af et organisk lag under ekstraktion er fordelagtigt, fordi:
* Det fremmer saltning , hvilket fører til et renere organisk lag.
* Det hjælper at reducere emulsionsdannelse , hvilket gør separationsprocessen lettere.
Deioniseret vand alene er mindre effektivt til disse formål.
Sidste artikelEr halogener opløselige i organisk opløsningsmiddel?
Næste artikelHvorfor opvarmes NaOH -ekstraktet før forsuring?
 Varme artikler
Varme artikler
-
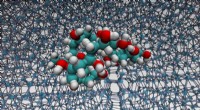 Løsning af puslespillet med polymerer, der binder sig til is til kryokonserveringEn detalje på molekylært niveau af interaktionen mellem PVA og is (fra molekylær dynamiksimuleringer). Kredit:University of Warwick Når biologisk materiale (celler, blod, væv) er frosset, kryobesk
Løsning af puslespillet med polymerer, der binder sig til is til kryokonserveringEn detalje på molekylært niveau af interaktionen mellem PVA og is (fra molekylær dynamiksimuleringer). Kredit:University of Warwick Når biologisk materiale (celler, blod, væv) er frosset, kryobesk -
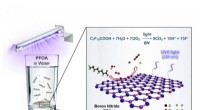 Bornitrid ødelægger for evigt kemikalier PFOA, GenXEn illustration af bornitrid-fotokatalyse, der ødelægger det forurenende stof PFOA i vand. Kredit:Billede udlånt af M. Wong/Rice University Rice University kemiingeniører fandt en effektiv katalys
Bornitrid ødelægger for evigt kemikalier PFOA, GenXEn illustration af bornitrid-fotokatalyse, der ødelægger det forurenende stof PFOA i vand. Kredit:Billede udlånt af M. Wong/Rice University Rice University kemiingeniører fandt en effektiv katalys -
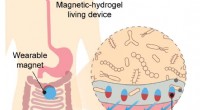 Levende sensorer undersøger tarmens mysterierSkematisk illustration af brugen af levende sensorer indkapslet i en magnetisk hydrogelanordning til undersøgelser af tarmen. Kredit:Xinyue Liu et al Forskning i den menneskelige tarm og mikrobe
Levende sensorer undersøger tarmens mysterierSkematisk illustration af brugen af levende sensorer indkapslet i en magnetisk hydrogelanordning til undersøgelser af tarmen. Kredit:Xinyue Liu et al Forskning i den menneskelige tarm og mikrobe -
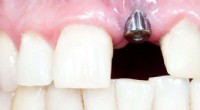 Radikale metoder til inficerede implantaterTandimplantater er mere og mere almindelige som erstatning for tænder i Norge. Udskiftningen kommer ikke altid uden problemer, imidlertid. Kredit:Colourbox.com Molekyler, der oftere er kendt for d
Radikale metoder til inficerede implantaterTandimplantater er mere og mere almindelige som erstatning for tænder i Norge. Udskiftningen kommer ikke altid uden problemer, imidlertid. Kredit:Colourbox.com Molekyler, der oftere er kendt for d
- Forskellen mellem enkle og sammensatte maskiner
- En modsat erklæring fra en hypotese er?
- Ny satellit har til formål at vise, hvordan AI fremmer jordobservation
- Kan du virkelig eje noget i metaversen? Hvordan blockchains og NFT'er ikke beskytter virtuel ejendom
- Hvordan bakterier binder deres usynlighedskapper til immunforsvaret
- Forskere tilbyder vejkort for at forbedre miljøobservationer i Det Indiske Ocean


