Er halogener opløselige i organisk opløsningsmiddel?
* Polaritet: Halogener (som fluor, klor, brom og jod) er ikke -polære molekyler. Organiske opløsningsmidler, som kulbrinter, er også generelt ikke -polære. "Ligesom opløser som" er en tommelfingerregel i kemi, hvilket betyder, at ikke -polære stoffer har en tendens til at opløses i ikke -polære opløsningsmidler.
* Intermolekylære kræfter: Halogener danner svage van der Waals -kræfter, som er de primære intermolekylære kræfter i organiske opløsningsmidler. Vand danner på den anden side stærke brintbindinger, hvilket gør det vanskeligt for ikke -polære halogener at opløses.
Eksempler:
* jod (i2) er let opløseligt i organiske opløsningsmidler som hexan, carbontetrachlorid og diethylether.
* klor (CL2) er opløseligt i organiske opløsningsmidler som chloroform og carbontetrachlorid.
Undtagelser:
* fluor (F2) er ekstremt reaktiv og kan reagere med mange organiske opløsningsmidler, hvilket gør det mindre sandsynligt, at det opløses på en enkel måde.
Kortfattet:
Halogener, der er ikke -polære, opløses godt i ikke -polære organiske opløsningsmidler på grund af lignende intermolekylære kræfter. De opløses generelt ikke i polære opløsningsmidler som vand.
 Varme artikler
Varme artikler
-
 Kemikere skaber en ny vej til PHA'er:naturligt nedbrydeligt bioplastFra venstre:kandidatstuderende Andrea Westlie, professor Eugene Chen, og forsker Xiaoyan Tang i Chemistry Research Building. Kredit:John Eisele En bølge af offentlig fremdrift svulmer op mod krise
Kemikere skaber en ny vej til PHA'er:naturligt nedbrydeligt bioplastFra venstre:kandidatstuderende Andrea Westlie, professor Eugene Chen, og forsker Xiaoyan Tang i Chemistry Research Building. Kredit:John Eisele En bølge af offentlig fremdrift svulmer op mod krise -
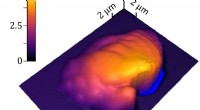 Ny metode måler 3-D polymerbearbejdning præcistEt 3D topografisk billede af en enkelt voxel af polymeriseret harpiks, omgivet af flydende harpiks. NIST-forskere brugte deres sample-coupled-resonance photo-rheology (SCRPR) teknik til at måle, hvord
Ny metode måler 3-D polymerbearbejdning præcistEt 3D topografisk billede af en enkelt voxel af polymeriseret harpiks, omgivet af flydende harpiks. NIST-forskere brugte deres sample-coupled-resonance photo-rheology (SCRPR) teknik til at måle, hvord -
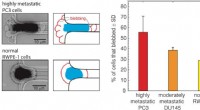 Ny teknik lover forbedret opdagelse af metastatisk prostatacancerTil venstre:Billeder af en blødende, stærkt metastaserende PC3 prostatacancercelle (øverst) og en ikke-blebbende normal RWPE-1 prostatacelle, der tvinges ind i en mikrofluidisk kanal. Midten:Omrids af
Ny teknik lover forbedret opdagelse af metastatisk prostatacancerTil venstre:Billeder af en blødende, stærkt metastaserende PC3 prostatacancercelle (øverst) og en ikke-blebbende normal RWPE-1 prostatacelle, der tvinges ind i en mikrofluidisk kanal. Midten:Omrids af -
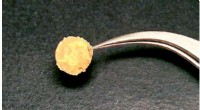 Ny teknik bygger superhårde metaller fra nanopartiklerDenne guldmønt blev lavet af byggesten i nanopartikler, takket være en ny teknik udviklet af Brown University -forskere. Fremstilling af bulkmetaller på denne måde muliggør præcis metalets mikrostrukt
Ny teknik bygger superhårde metaller fra nanopartiklerDenne guldmønt blev lavet af byggesten i nanopartikler, takket være en ny teknik udviklet af Brown University -forskere. Fremstilling af bulkmetaller på denne måde muliggør præcis metalets mikrostrukt
- Omprogrammerbar satellit sendt til opsendelsesstedet
- Hvilken type skærm er sammensat ekstremt tynde paneler organiske molekyler klemt mellem to elektrod…
- Hvad kredserer måner?
- Comcasts nye iPad-app til at vise tv-oversigter
- Er det skævt at adskille to væsker kogepunkter mindre end 5 grader?
- Undersøgelse fremhæver muligheden for at bygge bølgeformtolerante qubit-porte


