Hvad er polariteten af tert-butylchlorid?
* Elektronegativitetsforskel: Klor er signifikant mere elektronegativ end kulstof. Dette betyder, at klor tiltrækker de delte elektroner i C-CL-bindingen stærkere, hvilket skaber en delvis negativ ladning (Δ-) på kloratomet og en delvis positiv ladning (Δ+) på carbonatomet.
* molekylær geometri: Carbonatomet i tert-butylchlorid er bundet til fire grupper:tre methylgrupper og kloratomet. Dette resulterer i en tetrahedral geometri omkring kulstoffet, hvilket fører til en ujævn fordeling af elektrondensitet.
Generelt bidrager den polære C-CL-binding og den asymmetriske molekylære geometri til den polære karakter af tert-butylchlorid.
 Varme artikler
Varme artikler
-
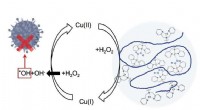 Ny strategi for lægemiddeldesign:At holde kobberatomer tættere på for at holde bakterier vækDen foreslåede polymer, med rygraden vist i blåt, skaber regioner med en høj lokal densitet af kobbersideenheder (vedhæng). Dette hjælper med at reducere Cu (II) til Cu (I), det vanskeligste trin i re
Ny strategi for lægemiddeldesign:At holde kobberatomer tættere på for at holde bakterier vækDen foreslåede polymer, med rygraden vist i blåt, skaber regioner med en høj lokal densitet af kobbersideenheder (vedhæng). Dette hjælper med at reducere Cu (II) til Cu (I), det vanskeligste trin i re -
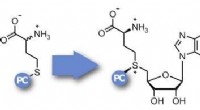 Enzymatisk photocaging til undersøgelse af genregulering gennem DNA-methyleringKredit:Wiley Tilføjelse og fjernelse af methylgrupper på DNA spiller en vigtig rolle i genregulering. For at studere disse mekanismer mere præcist, et tysk team har udviklet en ny metode, hvorved
Enzymatisk photocaging til undersøgelse af genregulering gennem DNA-methyleringKredit:Wiley Tilføjelse og fjernelse af methylgrupper på DNA spiller en vigtig rolle i genregulering. For at studere disse mekanismer mere præcist, et tysk team har udviklet en ny metode, hvorved -
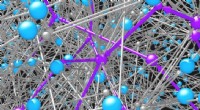 Deep learning -teknikker lærer neurale modeller at spille retrosynteseMolekyler (blå kugler) er forbundet med hinanden ved reaktionerne (grå kugler og pile), som de deltager i. Netværket af mulige organiske molekyler og reaktioner er umuligt stort. Intelligente søgealgo
Deep learning -teknikker lærer neurale modeller at spille retrosynteseMolekyler (blå kugler) er forbundet med hinanden ved reaktionerne (grå kugler og pile), som de deltager i. Netværket af mulige organiske molekyler og reaktioner er umuligt stort. Intelligente søgealgo -
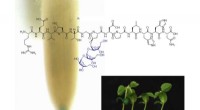 Modificerede peptider kunne booste plantevækst og udviklingNy undersøgelse viser, at peptider kan manipulere plantevækst, fører til højere udbytte. Kredit:Dr Brett Ferguson En ny australsk undersøgelse af peptidhormoner, der er kritiske for planteudviklin
Modificerede peptider kunne booste plantevækst og udviklingNy undersøgelse viser, at peptider kan manipulere plantevækst, fører til højere udbytte. Kredit:Dr Brett Ferguson En ny australsk undersøgelse af peptidhormoner, der er kritiske for planteudviklin
- Hvad ligger uden for gasgiganterne i solsystemet?
- Hvad er den molekylære formel for diphosphrøst pentoxid?
- Hvor mange elektroner vil et neutralt atom have, når det har 12 protoner?
- Lidt at fejre efter 50 års aktivisme:Greenpeace -chef
- Hvad er det sande forhold mellem tyngdekraft og bevægelse af vores solsystem?
- Hvor mange planet i universet?


