Hvilke kemiske arter indeholder alle elektrolytter?
Her er hvorfor:
* elektrolytter er stoffer, der udfører elektricitet, når de opløses i et opløsningsmiddel (normalt vand), eller når de er smeltet.
* ioner er atomer eller molekyler, der har vundet eller mistet elektroner, hvilket giver dem en nettopositiv eller negativ ladning.
* ledning af elektricitet Kræver bevægelse af ladede partikler. I elektrolytter er disse ladede partikler ioner.
Når en elektrolyt opløses, adskiller dens ioner sig og er fri til at bevæge sig, hvilket giver løsningen til at udføre elektricitet.
Eksempler:
* natriumchlorid (NaCl) opløses i natriumioner (Na+) og chloridioner (Cl-).
* kaliumhydroxid (KOH) opløses i kaliumioner (K+) og hydroxidioner (OH-).
Bemærk: Ikke alle ioniske forbindelser er elektrolytter. Nogle ioniske forbindelser er uopløselige og adskiller sig ikke i ioner i opløsning.
 Varme artikler
Varme artikler
-
 blidere, sikrere hårfarve baseret på syntetisk melaninEn mildere hårfarve baseret på syntetisk melanin kan producere en række farver, fra mørkebrun til rødguld. Kredit:Tilpasset fra ACS Central Science 2020, DOI:10.1021/acscentsci.0c00068 Med coron
blidere, sikrere hårfarve baseret på syntetisk melaninEn mildere hårfarve baseret på syntetisk melanin kan producere en række farver, fra mørkebrun til rødguld. Kredit:Tilpasset fra ACS Central Science 2020, DOI:10.1021/acscentsci.0c00068 Med coron -
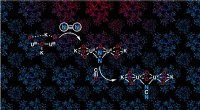 Nitrogenfiksering under omgivende forholdDen oxo-broforbundne uranforbindelse fanger dinitrogen og omdanner dinitrogen og kulilte til cyanamid. Kredit:Marta Falcone/Marinella Mazzanti/EPFL Rigelig i atmosfæren, kvælstof bruges sjældent t
Nitrogenfiksering under omgivende forholdDen oxo-broforbundne uranforbindelse fanger dinitrogen og omdanner dinitrogen og kulilte til cyanamid. Kredit:Marta Falcone/Marinella Mazzanti/EPFL Rigelig i atmosfæren, kvælstof bruges sjældent t -
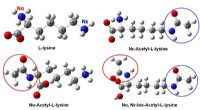 Raman og infrarød spektroskopi hjælper med at identificere forskellige acetylerede lysinerMolekylære strukturer af lysin og tre acetylerede lysiner. Kredit:Yao Guohua Et forskerhold ledet af prof. Huang Qing fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabs
Raman og infrarød spektroskopi hjælper med at identificere forskellige acetylerede lysinerMolekylære strukturer af lysin og tre acetylerede lysiner. Kredit:Yao Guohua Et forskerhold ledet af prof. Huang Qing fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabs -
 Automatisering af molekyledesign for at fremskynde lægemiddeludviklingMIT-forskere har udviklet en maskinlæringsmodel, der bedre udvælger molekylekandidater til terapi, samtidig med at det giver mulighed for automatiseret modifikation af den molekylære struktur for høje
Automatisering af molekyledesign for at fremskynde lægemiddeludviklingMIT-forskere har udviklet en maskinlæringsmodel, der bedre udvælger molekylekandidater til terapi, samtidig med at det giver mulighed for automatiseret modifikation af den molekylære struktur for høje
- Boeing sender Rosie dummy til rummet i en nøglemission uden besætning
- Hvad er nogle problemer med at bruge solenergi?
- Hvordan videnskabsmænd testede de supersoniske dynamiske egenskaber ved Tianwen-1 Mars Entry Capsul…
- Er en glasmikroskopobjektglasleder eller isolator hvorfor?
- Hvad findes en organelle i cytoplasmaet, der giver energi til celle?
- Forskning udforsker parametrene for det binære røntgensystem Scorpius X-1


