Hvad er atomstrukturen af klor?
Grundlæggende information
* atomnummer: 17 (dette betyder, at der er 17 protoner i kernen)
* atomisk symbol: Cl
* atommasse: 35.45 U (dette er den gennemsnitlige masse af alle klorisotoper)
struktur
* kerne:
* Protoner: 17 (positivt ladet)
* neutroner: 18 (Ingen afgift) - Dette er den mest almindelige isotop af klor. Der er andre isotoper med forskellige antal neutroner.
* Elektronskaller:
* 1. shell (k shell): 2 elektroner
* 2. shell (l shell): 8 elektroner
* 3. shell (m shell): 7 elektroner
nøglefunktioner
* Valenselektroner: De 7 elektroner i den yderste skal (M Shell) kaldes valenselektroner. Dette er de elektroner, der er involveret i kemisk binding.
* halogen: Chlor er en halogen, en gruppe af stærkt reaktive ikke -metaller, der let danner negative ioner (ANION) ved at få en elektron.
Hvorfor denne struktur betyder noget
* reaktivitet: Tilstedeværelsen af 7 valenselektroner gør chlor meget reaktiv, da den ønsker at få endnu en elektron for at afslutte sin ydre skal og opnå en stabil elektronkonfiguration som de ædle gasser.
* binding: Denne reaktivitet forklarer, hvorfor klor danner stærke bindinger med andre elementer, som i bordsalt (NaCl). Det får et elektron fra natrium og danner en negativ chloridion (Cl-), mens natrium mister et elektron for at blive en positiv natriumion (Na+).
Lad mig vide, om du vil have flere detaljer om specifikke aspekter af strukturen, såsom elektronkonfiguration eller isotopinformation.
 Varme artikler
Varme artikler
-
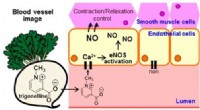 Forbindelser i monsterræddike kunne hjælpe med at tæmme hjerte-kar-sygdommeKredit:American Chemical Society Træd gulerødder til side, løg og broccoli. Den nyeste hjertesunde grøntsag kunne være en gigantisk, rekordsættende radise. I en undersøgelse, der vises i ACS Tids
Forbindelser i monsterræddike kunne hjælpe med at tæmme hjerte-kar-sygdommeKredit:American Chemical Society Træd gulerødder til side, løg og broccoli. Den nyeste hjertesunde grøntsag kunne være en gigantisk, rekordsættende radise. I en undersøgelse, der vises i ACS Tids -
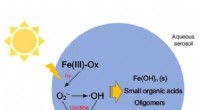 Virkninger af Fenton-lignende reaktioner af ferroloxalat på atmosfæriske oxidationsprocesser og st…Methacrolein reagerer med superoxidradikaler frembragt ved en Fenton-lignende reaktion. Dette påvirker atmosfærisk strålingsforcerende kraft på grund af dannelsen af uopløseligt jernhydroxid. Kredit
Virkninger af Fenton-lignende reaktioner af ferroloxalat på atmosfæriske oxidationsprocesser og st…Methacrolein reagerer med superoxidradikaler frembragt ved en Fenton-lignende reaktion. Dette påvirker atmosfærisk strålingsforcerende kraft på grund af dannelsen af uopløseligt jernhydroxid. Kredit -
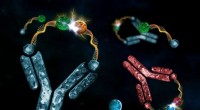 Sådan bruges antistoffer til at kontrollere kemiske reaktionerKunstnerisk fremstilling af to antistoffer, der udløser to kemiske reaktioner. Kredit:Oscar Melendre Hoyos I en samarbejdsindsats har en gruppe internationale forskere for nylig demonstreret en må
Sådan bruges antistoffer til at kontrollere kemiske reaktionerKunstnerisk fremstilling af to antistoffer, der udløser to kemiske reaktioner. Kredit:Oscar Melendre Hoyos I en samarbejdsindsats har en gruppe internationale forskere for nylig demonstreret en må -
 Team udvikler hurtig autentificeringsmetode for kinesisk medicinPolyUs forskerhold ledet af Dr Yao Zhongping, lektor ved Institut for Anvendt Biologi og Kemisk Teknologi, har udviklet en ny metode til hurtig autentificering af kinesisk urtemedicin, inklusive Lingz
Team udvikler hurtig autentificeringsmetode for kinesisk medicinPolyUs forskerhold ledet af Dr Yao Zhongping, lektor ved Institut for Anvendt Biologi og Kemisk Teknologi, har udviklet en ny metode til hurtig autentificering af kinesisk urtemedicin, inklusive Lingz
- Nævn nogle kræfter, der virker på et objekt i bevægelse?
- Hvordan planter og dyr interagerer i regnskoven
- Er det at ændre farve på en nellikskemisk eller fysisk forandring?
- Hvad ville være den korte konklusion for biologiprojekt, der er foretaget på oliespild?
- Sådan løses ligninger på isosceles-trekanter
- Et twist bringer nye muligheder for ultratynde 2D-materialer


