Hvad er den elektroniske struktur af en chloridion?
1. Udgangspunkt:kloratom
* Chlor (CL) har et atomnummer på 17, hvilket betyder, at det har 17 protoner og 17 elektroner.
* Dens elektroniske konfiguration er:1S² 2s² 2p⁶ 3S² 3P⁵
2. Dannelse af chloridion
* Klor vinder et elektron for at opnå en stabil octet (8 elektroner) i dets yderste skal.
* Dette skaber en negativ ladning, hvilket resulterer i chloridion (CL⁻).
3. Elektronisk konfiguration af chloridion
* Chloridionens elektroniske konfiguration bliver:1S² 2S² 2P⁶ 3S² 3P⁶
forenklet repræsentation:
* Chloridionen har en fuld ydre skal med 8 elektroner (2 i 3'erne orbital og 6 i 3p orbitaler).
* Dette giver det en stabil, ædel gaskonfiguration svarende til Argon (AR).
Nøglepunkter:
* Chloridionen er negativt ladet, fordi det har vundet en elektron.
* Dens elektroniske konfiguration er den samme som Argon, hvilket gør den meget stabil.
* Denne stabilitet er grunden til, at chloridioner er almindelige i ioniske forbindelser.
Sidste artikelHvad er den kemiske formel af Aqua-Regia?
Næste artikelHvad er navnet Molekyle CH3CH2CH2NH2?
 Varme artikler
Varme artikler
-
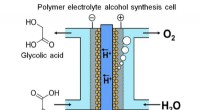 Udforskning af elektrolyse til energilagringEt forskningshold fra Kyushu University realiserede kontinuerlig elektrokemisk syntese af en alkoholisk forbindelse fra en carboxylsyre ved hjælp af en polymer elektrolyt alkohol elektrosyntesecelle,
Udforskning af elektrolyse til energilagringEt forskningshold fra Kyushu University realiserede kontinuerlig elektrokemisk syntese af en alkoholisk forbindelse fra en carboxylsyre ved hjælp af en polymer elektrolyt alkohol elektrosyntesecelle, -
 Defekt kulstof forenkler produktionen af brintoverilteForskere ved Rice University har introduceret plasmabehandlet kønrøg som en enkel og yderst effektiv katalysator til produktion af hydrogenperoxid. Defekter skabt i kulstoffet giver flere katalytiske
Defekt kulstof forenkler produktionen af brintoverilteForskere ved Rice University har introduceret plasmabehandlet kønrøg som en enkel og yderst effektiv katalysator til produktion af hydrogenperoxid. Defekter skabt i kulstoffet giver flere katalytiske -
 Identificeret:Molekylær struktur, der nedbryder en vigtig komponent i smogKredit:Pacific Northwest National Laboratory Kvælstofoxider, også kendt som NO x , dannes, når fossile brændstoffer brænder ved høje temperaturer. Når de udsendes fra industrielle kilder, såsom
Identificeret:Molekylær struktur, der nedbryder en vigtig komponent i smogKredit:Pacific Northwest National Laboratory Kvælstofoxider, også kendt som NO x , dannes, når fossile brændstoffer brænder ved høje temperaturer. Når de udsendes fra industrielle kilder, såsom -
 Nyopdaget materiale kan lette slitage på udenjordiske køretøjerKredit:Pixabay/CC0 Public Domain Mens NASAs Mars Perseverance Rover fortsætter med at udforske Mars overflade, forskere på Jorden har udviklet en ny nanoskala metalcarbid, der kunne fungere som et
Nyopdaget materiale kan lette slitage på udenjordiske køretøjerKredit:Pixabay/CC0 Public Domain Mens NASAs Mars Perseverance Rover fortsætter med at udforske Mars overflade, forskere på Jorden har udviklet en ny nanoskala metalcarbid, der kunne fungere som et
- Ny bog giver insiders syn på kosmisk søgen efter liv
- Hvordan modtager cellerne næringsstoffer fra mad?
- Arktisk tundra udsender mere metan under efterårets frysning end forårets optøning
- Carbon nanospike-katalysator spalter vand, kuldioxid og rekombinerer atomer til tungere nanocarboner
- Hvilke typer planteceller findes der?
- Hvordan påvirker nedbør mennesker?


