Udforskning af elektrolyse til energilagring
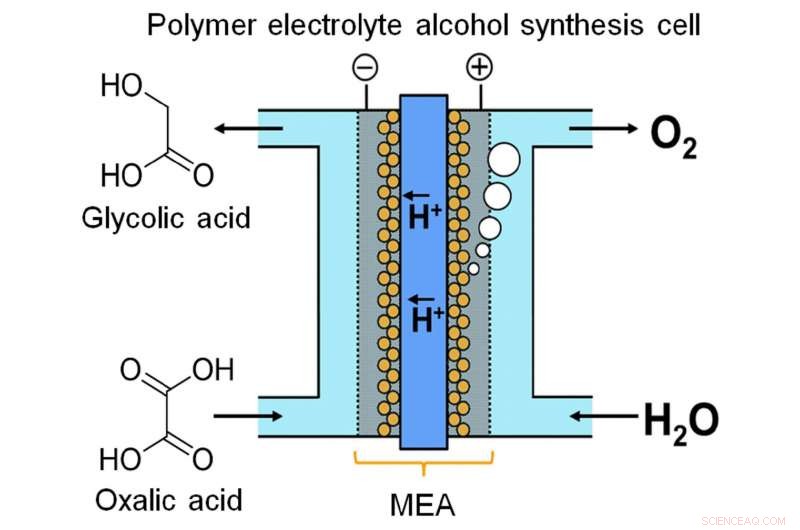
Et forskningshold fra Kyushu University realiserede kontinuerlig elektrokemisk syntese af en alkoholisk forbindelse fra en carboxylsyre ved hjælp af en polymer elektrolyt alkohol elektrosyntesecelle, som muliggør direkte strømladning til alkoholisk forbindelse. Kredit:Masaaki Sadakiyo / International Institute for Carbon-neutral Energy Research, Kyushu Universitet
Interessen for vedvarende energi fortsætter med at vokse. Mange vedvarende energikilder, selvom, kan være frustrerende intermitterende. Når solen er skjult af skyer, eller vinden holder op med at blæse, strømmen svinger. Den fluktuerende forsyning kan delvist udjævnes ved energilagring i spidsbelastningstider. Imidlertid, lagring af elektricitet er ikke uden udfordringer.
For nylig, et hold ved Kyushu University skabte en enhed til at lagre energi i kemisk form gennem kontinuerlig elektrolyse. Forskerne bemærkede, at glykolsyre (GC) har en meget større energikapacitet end brint, en af de mere populære energilagringskemikalier. GC kan fremstilles ved fire-elektron reduktion af oxalsyre (OX), en udbredt tilgængelig carboxylsyre. Som beskrevet i deres udgivelse i Videnskabelige rapporter , holdet udtænkte en elektrolytisk celle baseret på en ny membran-elektrode-samling. Indklemt mellem to elektroder er en iridiumoxid-baseret anode og en titaniumdioxid (TiO2)-coated titanium (Ti) katode, forbundet med en polymermembran.
"Flow-type systemer er meget vigtige for energilagring med væskefasereaktion, " siger hovedforfatter Masaaki Sadakiyo. "De fleste elektrolysatorer, der producerer alkoholer, driver en batchproces, som ikke er egnet til dette formål. I vores enhed, ved at bruge en fast polymerelektrolyt i direkte kontakt med elektroderne, vi kan køre reaktionen som et kontinuerligt flow uden tilsætning af urenheder (f.eks. elektrolytter). OX-løsningen kan effektivt opfattes som en flydende elektronpool."
En anden vigtig overvejelse er katodedesignet. Den katodiske reaktion katalyseres af anatase TiO2. For at sikre en solid forbindelse mellem katalysator og katode, holdet "voksede" TiO2 direkte på Ti i form af et net eller filt. Elektronmikroskopbilleder viser TiO2 som en tjavset fuzz, klamrer sig til ydersiden af Ti-stængerne som en belægning af nysne. Faktisk, dens opgave er at katalysere elektroreduktionen af OX til GC. I mellemtiden ved anoden, vand oxideres til oxygen.
Holdet fandt ud af, at reaktionen accelererede ved højere temperaturer. Imidlertid, at skrue for højt op for varmen opmuntrede til en uønsket biproces - omdannelsen af vand til brint. Den ideelle balance mellem disse to effekter var ved 60°C. Ved denne temperatur, enheden kan optimeres yderligere ved at bremse strømmen af reaktanter, samtidig med at mængden af overfladeareal, der er tilgængeligt for reaktionen, øges.
Interessant nok, selv teksturen af den uklare TiO2-katalysator gjorde en stor forskel. Da TiO2 blev fremstillet som en "filt, "ved at dyrke det på tyndere og tættere pakkede Ti-stænger, reaktionen skete hurtigere end på nettet - sandsynligvis på grund af det større overfladeareal. Filten modvirkede også brintproduktion, ved at dække Ti-overfladen mere tæt end nettet, forhindre eksponering af blottet Ti.
"Under de rette forhold, vores celle omdanner næsten 100 procent af OX, hvilket vi finder meget opmuntrende, " siger medforfatter Miho Yamauchi. "Vi beregner, at den maksimale volumetriske energikapacitet for GC-løsningen er omkring 50 gange brintgas. For at være klar, energieffektiviteten, i modsætning til kapacitet, stadig halter bagefter andre teknologier. Imidlertid, dette er et lovende første skridt til en ny metode til lagring af overskydende strøm."
 Varme artikler
Varme artikler
-
 Biokatalyse:Ny metode til at drive katalytisk aktive enzymerMarco Krewing, Abdulkadir Yayci og Julia Bandow forsker i muligheder for miljøvenlig katalyse med enzymer. Kredit:RUB, Marquard Et forskerhold fra Bochum har udviklet en ny metode til at drive kat
Biokatalyse:Ny metode til at drive katalytisk aktive enzymerMarco Krewing, Abdulkadir Yayci og Julia Bandow forsker i muligheder for miljøvenlig katalyse med enzymer. Kredit:RUB, Marquard Et forskerhold fra Bochum har udviklet en ny metode til at drive kat -
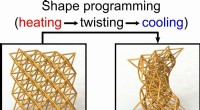 4-D-trykte materialer kan være stive som træ eller bløde som svamp4D-printede metamaterialer kan midlertidigt omdannes til enhver deformeret form og derefter returneres til deres oprindelige form efter behov, når de opvarmes. Skalaen er 2 millimeter. Kredit:Chen Yan
4-D-trykte materialer kan være stive som træ eller bløde som svamp4D-printede metamaterialer kan midlertidigt omdannes til enhver deformeret form og derefter returneres til deres oprindelige form efter behov, når de opvarmes. Skalaen er 2 millimeter. Kredit:Chen Yan -
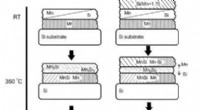 Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc
Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc -
 Brug af lasere til at visualisere molekylære mysterier i vores atmosfæreMolekylær vekselvirkning mellem gasser og væsker understøtter meget af vores liv, men vanskeligheder med at måle gas-væske kollisioner har indtil videre forhindret den grundlæggende udforskning af dis
Brug af lasere til at visualisere molekylære mysterier i vores atmosfæreMolekylær vekselvirkning mellem gasser og væsker understøtter meget af vores liv, men vanskeligheder med at måle gas-væske kollisioner har indtil videre forhindret den grundlæggende udforskning af dis
- Nyt gammelt havkrybdyr fundet i Tyskland – det tidligste af sin art
- Mikrober fester på knust klippe i subglaciale søer under Antarktis
- Hvorfor det er en dårlig idé at behandle vandknaphed som et sikkerhedsproblem
- Hvordan man bliver smartere i Math
- Forskere udvikler en ny måde at fjernmåle Jordens magnetfelt på
- Sentinel-2-hold forbereder sig på plads


