Hvad er en syre og typer syrer?
syrer:den sure sandhed
hvad er en syre?
I kemi er en syre et stof, der, når det opløses i vand, frigiver hydrogenioner (H+) og øger koncentrationen af disse ioner i opløsningen. Denne øgede koncentration af H+ -ioner giver syrer deres karakteristiske egenskaber, som en sur smag og evnen til at reagere med baser til dannelse af salte og vand.
Typer af syrer:
Syrer kan klassificeres baseret på deres styrke, kilde eller struktur:
1. Styrke:
* Stærke syrer: Disse adskiller sig fuldstændigt i vand og frigiver alle deres brintioner. Eksempler inkluderer:
* Saltsyre (HCL)
* Svovlsyre (H2SO4)
* Salpetersyre (HNO3)
* svage syrer: Disse adskiller sig kun delvist i vand og frigiver kun en lille del af deres brintioner. Eksempler inkluderer:
* Eddikesyre (CH3COOH) i eddike
* Citronsyre (C6H8O7) i citrusfrugter
* Kulsyre (H2CO3) i kulsyreholdige drikkevarer
2. Kilde:
* organiske syrer: Disse er afledt af levende organismer eller deres biprodukter. De indeholder typisk kulstof og findes ofte i frugt, grøntsager og andre naturlige kilder. Eksempler inkluderer:
* Citronsyre
* Mælkesyre
* Ascorbinsyre (C -vitamin)
* uorganinsyrer: Disse er ikke afledt af levende organismer. De indeholder typisk mineraler eller andre ikke-kulstofforbindelser. Eksempler inkluderer:
* Saltsyre
* Svovlsyre
* Salpetersyre
3. Struktur:
* monoprotiske syrer: Disse frigiver kun en hydrogenion pr. Molekyle, når de blev opløst i vand. Eksempel:HCL
* diprotiske syrer: Disse frigiver to hydrogenioner pr. Molekyle. Eksempel:H2SO4
* triprotiske syrer: Disse frigiver tre hydrogenioner pr. Molekyle. Eksempel:H3PO4
Vigtige noter:
* ph -skala: Asuriteten af en opløsning måles ved anvendelse af PH -skalaen, der varierer fra 0 til 14. syrer har en pH mindre end 7, mens baser har en pH -værdi større end 7.
* reaktioner: Syrer reagerer med baser for at danne salte og vand i en proces kaldet neutralisering. De reagerer også med metaller for at producere brintgas.
* sikkerhed: Stærke syrer er ætsende og kan forårsage alvorlige forbrændinger. Det er vigtigt at håndtere dem med forsigtighed og passende beskyttelsesudstyr.
Ved at forstå de forskellige typer syrer og deres egenskaber kan vi bedre forstå deres roller i forskellige kemiske processer og anvendelser, fra industriel produktion til hverdagen.
Sidste artikelHvad bruges svovldioxid til?
Næste artikelHvordan er uran saltbor og brint relateret?
 Varme artikler
Varme artikler
-
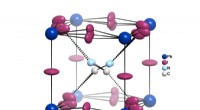 Perovskite solceller:Mulige aspekter af høj effektivitet afdækketTegningen illustrerer vekselvirkningen af den organiske methylammoniumkation (CH3NH3+) med de omgivende iodidioner. Skiftet af iodidatomerne ud af det fælles plan med bly forårsager brud på inversio
Perovskite solceller:Mulige aspekter af høj effektivitet afdækketTegningen illustrerer vekselvirkningen af den organiske methylammoniumkation (CH3NH3+) med de omgivende iodidioner. Skiftet af iodidatomerne ud af det fælles plan med bly forårsager brud på inversio -
 Metaller påvirker C-peptidhormon relateret til insulinUC Davis kemiker Marie Heffern er banebrydende på et nyt felt, metalloendokrinologi, at udforske, hvordan metaller som jern, zink og kobber påvirker hormoner. Kredit:Gregory Urquiaga/UC Davis Meta
Metaller påvirker C-peptidhormon relateret til insulinUC Davis kemiker Marie Heffern er banebrydende på et nyt felt, metalloendokrinologi, at udforske, hvordan metaller som jern, zink og kobber påvirker hormoner. Kredit:Gregory Urquiaga/UC Davis Meta -
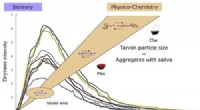 Hvorfor nogle rødvine smager tørtKredit:American Chemical Society Vinkendere kan nemt skelne mellem en tør rødvin, såsom Cabernet Sauvignon, fra en mere frugtbar rød, ligesom Pinot Noir. Forskere har længe forbundet følelsen af
Hvorfor nogle rødvine smager tørtKredit:American Chemical Society Vinkendere kan nemt skelne mellem en tør rødvin, såsom Cabernet Sauvignon, fra en mere frugtbar rød, ligesom Pinot Noir. Forskere har længe forbundet følelsen af -
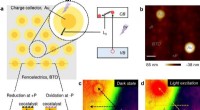 Forskere foreslår ny ladningsadskillelsesstrategi i ferroelektriske fotokatalysatorerLadningsadskillelse ved meta/ferroelektrisk grænseflade. et skematisk diagram af foreslået metal/ferroelektrisk fotokatalysator. b AFM-topografi af Au-partikler på en BaTiO3 enkelt krystal. Målestok,
Forskere foreslår ny ladningsadskillelsesstrategi i ferroelektriske fotokatalysatorerLadningsadskillelse ved meta/ferroelektrisk grænseflade. et skematisk diagram af foreslået metal/ferroelektrisk fotokatalysator. b AFM-topografi af Au-partikler på en BaTiO3 enkelt krystal. Målestok,
- Saltkoncentrationer i iskerner kunne afsløre opskriften på DO-begivenheder
- En 1000 kg bil, der rejser 25 miles i sekundet øst, har en kollision med 1500 kg varevogn oprindeli…
- Hvilken rolle spiller kobbersulfat i estimering ved iodometri?
- Studerendes forskerhold udvikler hybrid raketmotor
- Sådan fungerer tårnkraner
- Tidskrystaller leder forskere til fremtidigt beregningsarbejde


