Hvad er oxidationens halvreaktion af Cl2 2Cu til 2CUCL?
1. Identificer oxidationen
* kobber (cu) oxideres, fordi det går fra en elementær tilstand (0 oxidationstilstand) til en +1 oxidationstilstand i CUCL.
2. Skriv halvreaktionen
Oxidationen halvreaktion fokuserer kun på kobber:
Cu (s) → Cu⁺ (aq) + e⁻
Forklaring
* cu (s): Fast kobberatomer mister et elektron.
* cu⁺ (aq): Kobberioner i opløsning (vandig).
* e⁻: Det elektron, der går tabt.
Vigtig note: Chlor (CL₂) reduceres i denne reaktion, og du bliver nødt til at skrive en separat reduktion halvreaktion for fuldt ud at repræsentere den overordnede proces.
 Varme artikler
Varme artikler
-
 Kolloidale gelegenskaber under mikroskopetKredit:CC0 Public Domain Forskere ved University of Tokyo har udtænkt en metode til at følge gelering af kolloidale geler. Deres konfokalmikroskopiteknik har gjort det muligt at analysere de forsk
Kolloidale gelegenskaber under mikroskopetKredit:CC0 Public Domain Forskere ved University of Tokyo har udtænkt en metode til at følge gelering af kolloidale geler. Deres konfokalmikroskopiteknik har gjort det muligt at analysere de forsk -
 Brintkraft rykker et skridt nærmereFossile brændstoffer tegnede sig for næsten 90 procent af energiforbruget i 2015. Kredit:Lancaster University Fysikere ved Lancaster University udvikler metoder til at skabe vedvarende brændstof f
Brintkraft rykker et skridt nærmereFossile brændstoffer tegnede sig for næsten 90 procent af energiforbruget i 2015. Kredit:Lancaster University Fysikere ved Lancaster University udvikler metoder til at skabe vedvarende brændstof f -
 Ny forskning kan hjælpe renere energiteknologierGuangwen Zhou er professor i maskinteknik ved Binghamton University, State University of New York. Kredit:Binghamton University, State University of New York Ny forskning ledet af fakultetet ved B
Ny forskning kan hjælpe renere energiteknologierGuangwen Zhou er professor i maskinteknik ved Binghamton University, State University of New York. Kredit:Binghamton University, State University of New York Ny forskning ledet af fakultetet ved B -
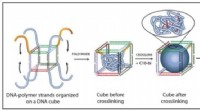 Ved hjælp af DNA -tråde til at designe nye polymermaterialerForskere fra McGill University har kemisk præget polymerpartikler med DNA-strenge - en teknik, der kan føre til nye materialer til anvendelser lige fra biomedicin til det lovende område blød robottekn
Ved hjælp af DNA -tråde til at designe nye polymermaterialerForskere fra McGill University har kemisk præget polymerpartikler med DNA-strenge - en teknik, der kan føre til nye materialer til anvendelser lige fra biomedicin til det lovende område blød robottekn
- Hvilke beviser er der, at planter fremstiller egen mad ved hjælp af energi fra solen?
- Vil ahorndage flytte sig fra marts til januar med global opvarmning?
- Hvilke ændringer har fundet sted i nåletræet?
- Nye RNA-nanoenheder i levende celler kan fornemme og analysere flere komplekse signaler
- Post-netneutralitet internet har brug for nye måleværktøjer, Princeton-eksperter fortæller polit…
- Er Mount ararat forbundet med Everest?


