Hvis X repræsenterer et element i gruppe 1, ville formlen, som dens oxid være, være, hvad?
Her er hvorfor:
* gruppe 1 elementer: Alkalimetaller har en valenselektron.
* ilt: Oxygen har brug for to elektroner for at opnå en stabil oktetkonfiguration.
* ionisk binding: Alkalimetaller mister let deres enkelt valenselektron til dannelse af en +1 -kation (x⁺). Oxygen får to elektroner til dannelse af en -2 anion (O⁻²).
* neutral forbindelse: For at skabe en neutral forbindelse har du brug for to x⁺ -kationer for at afbalancere -2 -ladningen af O⁻² -anionen, hvilket resulterer i formlen X₂O.
Eksempel: Natrium (NA) er et gruppe 1 -element. Dets oxid er Na₂o (natriumoxid).
Sidste artikelSkriv en COBOL PGM for at konvertere Celsius Fahrenheit?
Næste artikelHar oxidet af barium et højt eller lavt smeltepunkt?
 Varme artikler
Varme artikler
-
 Lys giver kontrol til 3D-udskrivning med flere materialerDe øverste billeder viser det digitale design og dets trykte form. Lilla svarer til ultraviolet hærdede stive epoxidområder, der henviser til, at de grå områder er synligt lyshærdede acrylatområder, d
Lys giver kontrol til 3D-udskrivning med flere materialerDe øverste billeder viser det digitale design og dets trykte form. Lilla svarer til ultraviolet hærdede stive epoxidområder, der henviser til, at de grå områder er synligt lyshærdede acrylatområder, d -
 Forbedret osteogen aktivitet af præ-osteoblaster på overflademodificerede 3-D printede stilladserTekniske materialeoverflader for maksimal cellelevedygtighed. Billedkredit:https://www.regenhu.com/3d-bio-printers Kredit:Biomedicinske materialer, doi:10.1088/1748-605x/aaeb82 Materialer såsom po
Forbedret osteogen aktivitet af præ-osteoblaster på overflademodificerede 3-D printede stilladserTekniske materialeoverflader for maksimal cellelevedygtighed. Billedkredit:https://www.regenhu.com/3d-bio-printers Kredit:Biomedicinske materialer, doi:10.1088/1748-605x/aaeb82 Materialer såsom po -
 Som fremtidige batterier, hybrid superkondensatorer er superladedeEt scanningselektronmikroskopibillede af vertikalt justerede kulstofnanorørelektroder belagt med titandisulfid aflejrede et atomlag ad gangen. Den forstørrede indsats viser individuelle titandisulfidb
Som fremtidige batterier, hybrid superkondensatorer er superladedeEt scanningselektronmikroskopibillede af vertikalt justerede kulstofnanorørelektroder belagt med titandisulfid aflejrede et atomlag ad gangen. Den forstørrede indsats viser individuelle titandisulfidb -
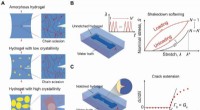 Anti-træthedsbrud hydrogelerDesignprincip for anti-træthedsbrud-hydrogeler. (A) Illustration af udmattelsesrevneudbredelse i en amorf hydrogel og i hydrogeler med lave og høje krystalliniteter under cykliske belastninger. De gul
Anti-træthedsbrud hydrogelerDesignprincip for anti-træthedsbrud-hydrogeler. (A) Illustration af udmattelsesrevneudbredelse i en amorf hydrogel og i hydrogeler med lave og høje krystalliniteter under cykliske belastninger. De gul
- To års nedtælling til minedrift på dyb havbund
- Hvad er nyt under solen? Forskere tilbyder et alternativt syn på, hvordan nye strukturer udvikler s…
- Stigende temperaturer ændrer, hvornår og hvor meget folk kommer ud på offentlige arealer
- Hvad er mængden af måne, der altid tændes undtagen under en måneformørkelse?
- Sådan konverteres rørstørrelse til GPM
- Hvad er nogle argumenter imod bevaring?


