Hvad er forskellen mellem vanddampmolekyler og flydende molekyler?
* vanddampmolekyler er individuelle H₂O -molekyler, der er langt fra hinanden og flyt frit og hurtigt , der sprænger hinanden med minimal tiltrækning. Dette er fordi de har høj kinetisk energi og er i en gasformig tilstand .
* flydende vandmolekyler er også H₂O -molekyler, men de er tættere sammen og flyt langsommere med en konstant, tilfældig bevægelse . Dette skyldes, at intermolekylære kræfter Mellem dem er stærkere end molekylernes kinetiske energi, der holder dem i en flydende tilstand .
Her er en mere detaljeret sammenbrud:
Vanddamp:
* tilstand: Gas
* afstand: Molekyler er langt fra hinanden
* Bevægelse: Molekyler bevæger sig frit og hurtigt
* Intermolekylære kræfter: Svag
* kinetisk energi: Høj
flydende vand:
* tilstand: Flydende
* afstand: Molekyler er tættere sammen
* Bevægelse: Molekyler bevæger sig langsommere, med tilfældig bevægelse
* Intermolekylære kræfter: Stærk
* kinetisk energi: Moderat
Tænk på det sådan:
* Vanddamp: Forestil dig en travl skare af mennesker, der alle løber rundt i et stort, åbent rum.
* flydende vand: Forestil dig de samme mennesker pakket tæt sammen i et overfyldt rum, der bevæger sig langsommere, men stadig konstant støder på hinanden.
Forskellen mellem vanddamp og flydende vand skyldes primært mængden af energi Molekylerne har. Med mere energi bevæger molekyler sig hurtigere og bryder sig fri fra intermolekylære kræfter og danner en gas. Med mindre energi bevæger de sig langsommere og holdes sammen af intermolekylære kræfter og danner en væske.
Sidste artikelEr natriummetal et element eller forbindelse?
Næste artikelHvilke egenskaber har svovl?
 Varme artikler
Varme artikler
-
 Forskere har opdaget, hvordan blodorme fremstiller deres unikke kobbertænderVenstre:Billede af den udbøjede snabel af Glycera dibranchiata med dens fire fritlagte kæber, højre:Scanningselektronmikroskopbillede af en Glycera-kæbe (Skalastang, 0,5 mm). Kredit:Matter/Wonderly et
Forskere har opdaget, hvordan blodorme fremstiller deres unikke kobbertænderVenstre:Billede af den udbøjede snabel af Glycera dibranchiata med dens fire fritlagte kæber, højre:Scanningselektronmikroskopbillede af en Glycera-kæbe (Skalastang, 0,5 mm). Kredit:Matter/Wonderly et -
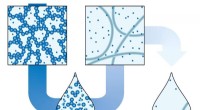 Kemikere finder en modsat effekt:Hvordan fortynding med vand gør en opløsning fastGrafisk fremstilling af faseovergange. Kredit:Koen Pieterse I Videnskab , TU/e-forskere har offentliggjort deres undersøgelse om nye faseovergange af opløsninger og geler i vand, som ser ud til at
Kemikere finder en modsat effekt:Hvordan fortynding med vand gør en opløsning fastGrafisk fremstilling af faseovergange. Kredit:Koen Pieterse I Videnskab , TU/e-forskere har offentliggjort deres undersøgelse om nye faseovergange af opløsninger og geler i vand, som ser ud til at -
 Beetle-vægte holder hemmeligheden bag at skabe bæredygtig maling af genbrugsplastik, forskning vis…Foto af to cyphochilus biller. Kredit:Olimpia1lli - CC BY-SA 4.0 Strukturen af ultrahvide billevægte kunne være nøglen til at fremstille lyshvid bæredygtig maling ved hjælp af genbrugsplastikaff
Beetle-vægte holder hemmeligheden bag at skabe bæredygtig maling af genbrugsplastik, forskning vis…Foto af to cyphochilus biller. Kredit:Olimpia1lli - CC BY-SA 4.0 Strukturen af ultrahvide billevægte kunne være nøglen til at fremstille lyshvid bæredygtig maling ved hjælp af genbrugsplastikaff -
 Computermodel til design af proteinsekvenser, der er optimeret til at binde til lægemiddelmålVed at bruge en computermodelleringstilgang, som de udviklede, MIT-biologer identificerede tre forskellige proteiner, der kan binde selektivt til hver af tre lignende mål, alle medlemmer af Bcl-2-fami
Computermodel til design af proteinsekvenser, der er optimeret til at binde til lægemiddelmålVed at bruge en computermodelleringstilgang, som de udviklede, MIT-biologer identificerede tre forskellige proteiner, der kan binde selektivt til hver af tre lignende mål, alle medlemmer af Bcl-2-fami
- NASA ser den tropiske depression Khanun sissipere i Tonkin-bugten
- Gaza-krigen:Hvordan efterforskere ville gå om at finde og verificere underjordiske militærkompleks…
- Nye isolatorer med ledende kanter
- NEEMO:Test af rumudstyr under havet
- Hvilke kategorier hører din sol til?
- Byggeplads for molekylære komplekser


