Hvad er forbindelsen af PBL4?
Her er hvorfor:
* bly (pb) Former typisk to almindelige oxidationstilstande:+2 og +4.
* jod (i) er en halogen og danner typisk en anion med en -1 -ladning (i⁻).
For at afbalancere ladningerne skal bly være i dens +4 oxidationstilstand for at kombinere med fire iodidioner. Lead er imidlertid mere stabil i dens +2 oxidationstilstand. Dette betyder, at forbindelsen pbi₂ (bly (II) iodid) er den mere sandsynlige og stabile forbindelse.
Sidste artikelHvad er handlingen af H2O2 på KMNO4?
Næste artikelHvilken type binding vil sandsynligvis dannes fra jern og svovl?
 Varme artikler
Varme artikler
-
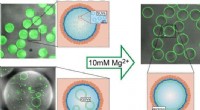 Cellelignende lipidvesikler, som kan udfyldes med naturlige celleproteinerLipidvesikler (til venstre:LUVer eller GUVer; grøn) blev indkapslet i copolymerstabiliserede dråber. Vesiklerne kan transformeres til et lipid-dobbeltlag ved den copolymerstabiliserede dråbe indre græ
Cellelignende lipidvesikler, som kan udfyldes med naturlige celleproteinerLipidvesikler (til venstre:LUVer eller GUVer; grøn) blev indkapslet i copolymerstabiliserede dråber. Vesiklerne kan transformeres til et lipid-dobbeltlag ved den copolymerstabiliserede dråbe indre græ -
 Nye metamaterialer omdannes til nye former, overtager nye ejendommeEt nanoarchitected metamateriale deformerer for at oprette Caltech -ikonet. Kredit:Julia Greer/Caltech En nyudviklet type arkitekteret metamateriale har evnen til at ændre form på en afstemt måde.
Nye metamaterialer omdannes til nye former, overtager nye ejendommeEt nanoarchitected metamateriale deformerer for at oprette Caltech -ikonet. Kredit:Julia Greer/Caltech En nyudviklet type arkitekteret metamateriale har evnen til at ændre form på en afstemt måde. -
 Bæredygtigt biomedicinsk udstyr til brug i regenerativ medicinKredit:CC0 Public Domain UPV/EHU-forskere har udviklet et biomedicinsk apparat, der består af biprodukter fra fødevareindustrien, og som udviser fremragende egenskaber til brug i regenerativ medic
Bæredygtigt biomedicinsk udstyr til brug i regenerativ medicinKredit:CC0 Public Domain UPV/EHU-forskere har udviklet et biomedicinsk apparat, der består af biprodukter fra fødevareindustrien, og som udviser fremragende egenskaber til brug i regenerativ medic -
 Et molekylært kig på begyndende HDL-dannelseForskere ved Boston University brugte en trunkeret version af Apolipoprotein A-I, vist her, at fastslå endegyldigt, at proteinet skal bindes til lipidtransportøren ABCA1 for at begynde at danne high-d
Et molekylært kig på begyndende HDL-dannelseForskere ved Boston University brugte en trunkeret version af Apolipoprotein A-I, vist her, at fastslå endegyldigt, at proteinet skal bindes til lipidtransportøren ABCA1 for at begynde at danne high-d
- Sådan renser du New Delhis smoggy luft
- Betydningen af hypotese-test
- Hvad skal man gøre ved et hundeangreb, og hvorfor de hader postarbejdere så meget
- IMERG viser ødelæggende nedbør over Østafrika
- What is a substance that allows electricity to pass through it easily?
- Hvornår blev Galileo -termometer opfundet?


