Hvad er den korrekte formel og ladning for en ion af nitrat?
Her er hvorfor:
* nitrogen (n) er i gruppe 15 i den periodiske tabel, hvilket betyder, at den typisk danner tre obligationer.
* ilt (O) er i gruppe 16, hvilket betyder, at det typisk danner to obligationer.
* For at opnå en stabil oktet deler nitrogen sine tre valenselektroner med tre iltatomer.
* Et af iltatomerne danner en dobbeltbinding med nitrogen, mens de to andre danner enkeltbindinger.
* Nitrogenatomet har en formel ladning på +1, og hver af de enkeltbundne iltatomer har en formel afgift på -1.
* Den samlede ladning af nitrationen er derfor -1 .
Sidste artikelVed hvilken temperatur bliver ilt en væske?
Næste artikelForklar hvorfor benzen C6H6 har et lavere kogepunkt end vand?
 Varme artikler
Varme artikler
-
 Solsiden opad:Kan du virkelig stege et æg på gangstien på en varm dag?Kredit:Shutterstock Aahh, den australske sommer. Når temperaturerne topper 40℃, og kun de modigste eller mest dumdristige ville vove sig udenfor på bare fødder, er der et elsket gammelt ordsprog:de
Solsiden opad:Kan du virkelig stege et æg på gangstien på en varm dag?Kredit:Shutterstock Aahh, den australske sommer. Når temperaturerne topper 40℃, og kun de modigste eller mest dumdristige ville vove sig udenfor på bare fødder, er der et elsket gammelt ordsprog:de -
 Forskere opfinder processen til fremstilling af bæredygtigt gummi, plastikVores team kombinerede en katalysator, vi for nylig har opdaget, med ny og spændende kemi for at finde det første høje udbytte, lavprismetode til fremstilling af butadien, siger Dionisios Vlachos, Dir
Forskere opfinder processen til fremstilling af bæredygtigt gummi, plastikVores team kombinerede en katalysator, vi for nylig har opdaget, med ny og spændende kemi for at finde det første høje udbytte, lavprismetode til fremstilling af butadien, siger Dionisios Vlachos, Dir -
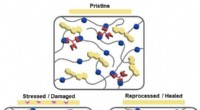 Skaderrapporterende og selvhelbredende hudlignende polymerbelægningerSkematisk af mekanokromiske og selvhelbredende termohærder. Kredit:Korea Institute of Science and Technology (KIST) Hudlignende polymerbelægninger påføres overfladerne af biler, skibe og bygninger
Skaderrapporterende og selvhelbredende hudlignende polymerbelægningerSkematisk af mekanokromiske og selvhelbredende termohærder. Kredit:Korea Institute of Science and Technology (KIST) Hudlignende polymerbelægninger påføres overfladerne af biler, skibe og bygninger -
 Hydrogel baner vejen for biomedicinsk gennembrudDr Behnam Akhavan, Universitetet i Sydney. Kredit:University of Sydney Udgivet i Avancerede funktionelle materialer , et team af biomedicinske ingeniører fra University of Sydney har udviklet en
Hydrogel baner vejen for biomedicinsk gennembrudDr Behnam Akhavan, Universitetet i Sydney. Kredit:University of Sydney Udgivet i Avancerede funktionelle materialer , et team af biomedicinske ingeniører fra University of Sydney har udviklet en


