Hvilket element har karakteristika, der mest ligner fluor?
Her er hvorfor:
* de er begge halogener: Dette betyder, at de hører til gruppe 17 i den periodiske tabel og deler lignende kemiske egenskaber.
* Lignende elektronegativitet: Både fluor og klor er meget elektronegative, hvilket betyder, at de har en stærk tendens til at tiltrække elektroner.
* Lignende reaktivitet: Fluor er den mest reaktive ikke -metale, mens klor er den næst mest reaktive. Begge danner let ioniske forbindelser og er gode oxidationsmidler.
* Lignende elektronkonfiguration: Både fluor og klor har 7 valenselektroner, hvilket giver dem lignende bindingsmønstre.
Det er dog vigtigt at bemærke, at klor er mindre reaktiv og har en lavere elektronegativitet end fluor. Dette skyldes, at klor er større i størrelse, hvilket fører til en svagere tiltrækning mellem kernen og dens yderste elektroner.
 Varme artikler
Varme artikler
-
 RES URBIS-projektet viser levedygtigheden af bioplastproduktion med bioaffald fra byerEn prøve af det brugte affald, det taget produkt fra bakterievirkning, samt flere indhentede bioplastprodukter i projektet. Kredit:J. Mata/UB I en cirkulær økonomi, byaffald bliver omdannet til re
RES URBIS-projektet viser levedygtigheden af bioplastproduktion med bioaffald fra byerEn prøve af det brugte affald, det taget produkt fra bakterievirkning, samt flere indhentede bioplastprodukter i projektet. Kredit:J. Mata/UB I en cirkulær økonomi, byaffald bliver omdannet til re -
 Gennembrudssensor til at hjælpe mennesker med bipolar lidelse med at overvåge litiumniveauerKredit:University of Surrey Patienter, der lever med bipolar lidelse og depression, vil snart kunne bruge en unik bærbar sensor til sikkert at overvåge deres litiumniveau. I en undersøgelse udgiv
Gennembrudssensor til at hjælpe mennesker med bipolar lidelse med at overvåge litiumniveauerKredit:University of Surrey Patienter, der lever med bipolar lidelse og depression, vil snart kunne bruge en unik bærbar sensor til sikkert at overvåge deres litiumniveau. I en undersøgelse udgiv -
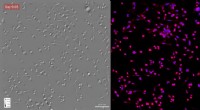 Ny metode bruger kunstig intelligens til at studere levende cellerTime-lapse gradient lysinterferensmikroskopi, eller GLIM, venstre, og fasebilleddannelse med beregningsspecificitet afbildet over syv dage. Kredit:Beckman Institute for Advanced Science and Technology
Ny metode bruger kunstig intelligens til at studere levende cellerTime-lapse gradient lysinterferensmikroskopi, eller GLIM, venstre, og fasebilleddannelse med beregningsspecificitet afbildet over syv dage. Kredit:Beckman Institute for Advanced Science and Technology -
 Venstre eller højre molekyler giver en hånd til materielle strukturerEn rekonstruktion af blokcopolymerer set gennem et elektronmikroskop viser tydeligt, hvordan de følger chiraliteten, eller håndfasthed, etableret af deres grundlæggende molekyler og vokser til spiralf
Venstre eller højre molekyler giver en hånd til materielle strukturerEn rekonstruktion af blokcopolymerer set gennem et elektronmikroskop viser tydeligt, hvordan de følger chiraliteten, eller håndfasthed, etableret af deres grundlæggende molekyler og vokser til spiralf
- Hvilket kort ville du bruge til at finde Afrikas ørkener?
- Ingen hurtig løsning tilgængelig for effektiv risikostyring i organisationer
- Du voksede i en hule, men du lever ikke i live begyndte vand, og mineraler nu ser solid aldrig himle…
- Hvad er den gas, der brænder for at danne vand?
- Forskere skaber molekyle til at tackle antimikrobiel resistens
- Hvad ville der ske, hvis den polære akse vinkelret var vinkelret på planet bane i stedet 23,5 grad…


