Beregn molariteten af en opløsning, der indeholder 35,0 g bariumchlorid opløst i 450,0 ml opløsning?
1. Konverter gram med opløst stof til mol:
* Find den molære masse af bariumchlorid (bacl₂):
* Barium (BA):137,33 g/mol
* Chlor (CL):35,45 g/mol (x2 for to kloratomer)
* Molmasse af bacl₂ =137,33 + (35,45 x 2) =208,23 g/mol
* Opdel massen af bariumchlorid med dets molære masse for at finde molerne:
* Mol bacl₂ =35,0 g / 208,23 g / mol =0,168 mol
2. Konverter milliliter af løsning til liter:
* Opdel volumen i ml med 1000:
* Liter opløsning =450,0 ml / 1000 ml / l =0,450 l
3. Beregn molaritet:
* Molaritet (M) er defineret som mol af opløst stof pr. Liter opløsning:
* Molaritet =mol bacl₂ / liter opløsning
* Molaritet =0,168 mol / 0,450 L
* Molaritet = 0,373 m
Derfor er molariteten af bariumchloridopløsningen 0,373 m.
Sidste artikelHvorfor kloroxid har et lavt smeltepunkt?
Næste artikelDen mest almindelige form for brint har?
 Varme artikler
Varme artikler
-
 High-throughput computermodel forudsiger diffusionsdata for transporten af lette elementer i faste…Kredit:CC0 Public Domain Spredningen af lette elementer til metaller er blevet effektivt modelleret af A*STAR-forskere ved hjælp af en maskinlæringstilgang. Faststofdiffusion, hvor atomer migre
High-throughput computermodel forudsiger diffusionsdata for transporten af lette elementer i faste…Kredit:CC0 Public Domain Spredningen af lette elementer til metaller er blevet effektivt modelleret af A*STAR-forskere ved hjælp af en maskinlæringstilgang. Faststofdiffusion, hvor atomer migre -
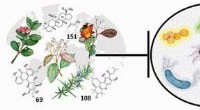 Gennemgang af planternes rolle i antibakteriel aktivitet rydder nye veje til opdagelse af lægemidle…Kredit:Emory University Forskere har samlet den første omfattende gennemgang af plante naturlige produkter, der spiller en rolle i antibakteriel aktivitet, at tjene som vejledning i søgen efter ny
Gennemgang af planternes rolle i antibakteriel aktivitet rydder nye veje til opdagelse af lægemidle…Kredit:Emory University Forskere har samlet den første omfattende gennemgang af plante naturlige produkter, der spiller en rolle i antibakteriel aktivitet, at tjene som vejledning i søgen efter ny -
 Udvikling af en ny billig galliumnitrid (GaN) krystalfremstillingsenhedUdseende af THVPE krystalvækstovn. Kredit:Taiyo Nippon Sanso Co. JST annoncerer den succesrige udvikling af en højkvalitets bulk GaN vækstenhed baseret på THVPE-metoden, et udviklingsemne for det
Udvikling af en ny billig galliumnitrid (GaN) krystalfremstillingsenhedUdseende af THVPE krystalvækstovn. Kredit:Taiyo Nippon Sanso Co. JST annoncerer den succesrige udvikling af en højkvalitets bulk GaN vækstenhed baseret på THVPE-metoden, et udviklingsemne for det -
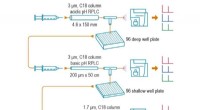 Forbedret proteinanalyse kan hjælpe med tidlig sygdomsdetektionPNNLs dybdyk-SRM-metode tilbyder en ny måde at forberede og analysere blodprøver på, og gør det muligt at påvise proteiner, der findes i meget lave koncentrationer – så lidt som 10 pikogram pr. millil
Forbedret proteinanalyse kan hjælpe med tidlig sygdomsdetektionPNNLs dybdyk-SRM-metode tilbyder en ny måde at forberede og analysere blodprøver på, og gør det muligt at påvise proteiner, der findes i meget lave koncentrationer – så lidt som 10 pikogram pr. millil
- Hvordan ved forskerne om månen?
- Kvanteffekter i nanotråde ved stuetemperatur
- Mikrotyngdekraft efter behov med Jordens tilbagevenden gennem ESAs Boost
- Hvorfor er syre vigtig?
- Hvad er fordelen ved at bruge lov i feltfysik i stedet
- Hvad sker der med plante- og dyerceller, når de placeres i hypertoniske, hypotoniske og isotoniske …


