Hvis to kloratomer skulle tiltrække elektroner fra calcium, ville de blive ladet?
* klorens natur: Kloratomer har en høj elektronegativitet, hvilket betyder, at de har en stærk attraktion for elektroner.
* Calciums natur: Calciumatomer har en lav elektronegativitet, hvilket betyder, at de er mere tilbøjelige til at miste elektroner.
* ionisk binding: Når chloratomer tiltrækker elektroner fra calcium, får de en negativ ladning og bliver chloridioner (Cl-). Calcium mister elektroner og bliver en positivt ladet calciumion (Ca2+).
* Elektrostatisk attraktion: De modsatte ladninger af ionerne skaber en stærk elektrostatisk attraktion, der danner en ionisk binding. Dette er grundlaget for forbindelseskalciumchlorid (CACL2).
Kortfattet: Chloratomerne ville blive negativt ladede chloridioner (Cl-), når de tiltrækker elektroner fra calcium.
 Varme artikler
Varme artikler
-
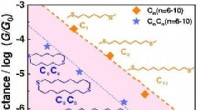 Stærkt isolerende alkanringe med destruktiv σ-interferensDe blå stjernetegn på mættede alkanringe viser eksponentielt henfaldskonduktans, og henfaldstendensen ligner mættede alkankæder, som præsenteres af orange firkanter. Alkanringene er mere isolerende en
Stærkt isolerende alkanringe med destruktiv σ-interferensDe blå stjernetegn på mættede alkanringe viser eksponentielt henfaldskonduktans, og henfaldstendensen ligner mættede alkankæder, som præsenteres af orange firkanter. Alkanringene er mere isolerende en -
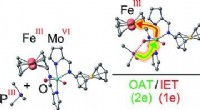 Bioinspireret enzymmodel med redox -switchKredit:Wiley Koblede oxygenoverførsler og elektronoverførselsreaktioner, der anvender kofaktorer, er enzymatiske reaktioner af afgørende betydning for alle livsformer fra bakterier til hvirveldyr.
Bioinspireret enzymmodel med redox -switchKredit:Wiley Koblede oxygenoverførsler og elektronoverførselsreaktioner, der anvender kofaktorer, er enzymatiske reaktioner af afgørende betydning for alle livsformer fra bakterier til hvirveldyr. -
 Skabelon til at skabe superatomer kunne give bedre batterierKredit:ktsdesign, Shutterstock Virginia Commonwealth University-forskere har opdaget en ny strategi til at skabe superatomer - kombinationer af atomer, der kan efterligne egenskaberne af mere end
Skabelon til at skabe superatomer kunne give bedre batterierKredit:ktsdesign, Shutterstock Virginia Commonwealth University-forskere har opdaget en ny strategi til at skabe superatomer - kombinationer af atomer, der kan efterligne egenskaberne af mere end -
 Hvordan fiskeskind og alger kunne hjælpe med at løse plastikforureningskrisenProduktdesignstuderende Lucy Hughes har opfundet en bioplast skabt af fiskeskind og skæl og røde alger. Kredit:University of Sussex En studerende fra University of Sussex har hentet inspiration fr
Hvordan fiskeskind og alger kunne hjælpe med at løse plastikforureningskrisenProduktdesignstuderende Lucy Hughes har opfundet en bioplast skabt af fiskeskind og skæl og røde alger. Kredit:University of Sussex En studerende fra University of Sussex har hentet inspiration fr
- Hvad sker der, når kulbrinter reagerer med zinkoxid?
- Bygninger:Det ubrydelige bånd
- Hvor er den gamle fyr i pergament ørken fossile krigere?
- Hvordan ved videnskabsmænd, hvornår de har de rigtige svar?
- Den evolutionære oprindelse til, hvorfor du er programmeret til at elske sukker
- Hvorfor har månen en del i formørkelser?


