Hvilken forbindelse er PBCL3?
Her er hvorfor:
* bly (pb) Former typisk to almindelige ioner:Pb²⁺ (bly (II)) og PB⁴⁺ (bly (IV)).
* klor (Cl) danner en -1 ion (cl⁻).
* For at afbalancere ladninger i en forbindelse skal de samlede positive afgifter svare til de samlede negative afgifter.
* For PBCL3 har vi brug for en Pb³⁺ -ion, som ikke er en almindelig oxidationstilstand for bly.
De almindelige blychloridforbindelser er:
* bly (ii) chlorid (PBCL₂) :Dette er et hvidt fast stof, der ofte bruges i laboratorieeksperimenter.
* bly (IV) chlorid (PBCL₄) :Dette er en meget ustabil forbindelse og nedbrydes let.
Derfor er PBCL3 ikke en kendt eller stabil forbindelse.
Sidste artikelHvor mange atomer i 10 mol NA?
Næste artikelHvad er fordele og ulemper ved Uranium-238?
 Varme artikler
Varme artikler
-
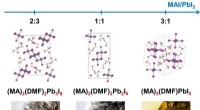 Forskere foreslår metode til at øge effektiviteten af solcellebatterierKrystalstrukturer af krystallinske solvater. Kredit:Alexey Tarasov Forskere fra Institut for Materialevidenskab, Lomonosov MSU, har bestemt, hvordan ændring af forholdet mellem komponenter, der da
Forskere foreslår metode til at øge effektiviteten af solcellebatterierKrystalstrukturer af krystallinske solvater. Kredit:Alexey Tarasov Forskere fra Institut for Materialevidenskab, Lomonosov MSU, har bestemt, hvordan ændring af forholdet mellem komponenter, der da -
 Gennembrud inden for ligninforskning - sfæriske partikler formerer enzymeffektivitetenBiokatalysatorer (billedet i bunden af hætteglasset), understøttet af sfæriske ligninpartikler og indlejret i naturlig polymermatrix, åbne nye veje til grønne syntesereaktioner i nærvær af vand. Kre
Gennembrud inden for ligninforskning - sfæriske partikler formerer enzymeffektivitetenBiokatalysatorer (billedet i bunden af hætteglasset), understøttet af sfæriske ligninpartikler og indlejret i naturlig polymermatrix, åbne nye veje til grønne syntesereaktioner i nærvær af vand. Kre -
 Flydende metaller de hemmelige ingredienser til at rense miljøetKredit:CC0 Public Domain Glem laboratoriet, stoffer, der kan løse miljøproblemer ved at opfange kuldioxid, dekontaminering af vand og oprensning af forurenende stoffer kan nemt skabes i et køkken,
Flydende metaller de hemmelige ingredienser til at rense miljøetKredit:CC0 Public Domain Glem laboratoriet, stoffer, der kan løse miljøproblemer ved at opfange kuldioxid, dekontaminering af vand og oprensning af forurenende stoffer kan nemt skabes i et køkken, -
 Mindre fugt i naturlige fibreFor at gøre de naturlige fibre mere modstandsdygtige, rovingen er imprægneret med monomerer:polymerisationen fortsætter derefter inde i garnet. Kredit:Fraunhofer LBF Naturfibre har mange fordele:d
Mindre fugt i naturlige fibreFor at gøre de naturlige fibre mere modstandsdygtige, rovingen er imprægneret med monomerer:polymerisationen fortsætter derefter inde i garnet. Kredit:Fraunhofer LBF Naturfibre har mange fordele:d
- Hvor kan man se månen mest tydeligt på nattehimlen?
- Den sovjetiske kosmonaut lavede banebrydende rumfart for 60 år siden
- Hvad er kilden til magt i en rumfærgen?
- Twitters skæbne:at forblive lille? Ikke så hurtigt, siger investorer
- New York mærker stadig virkningerne af orkanen Sandy, fem år senere
- Skovplanter og dyr


