Hvor mange mol ilt i 30L gas?
Her er hvorfor:
* den ideelle gaslov: Forholdet mellem volumen, tryk, temperatur og mol af en gas beskrives af den ideelle gaslov:
* pv =nrt
* p: Tryk (i atmosfærer)
* v: Volumen (i liter)
* n: Antal mol
* r: Ideel gaskonstant (0,0821 L · ATM/Mol · K)
* t: Temperatur (i Kelvin)
* Løsning for mol (n): For at finde antallet af mol (n) omarrangerer vi ligningen:
* n =pv / rt
For at beregne molen af ilt i 30L gas skal du tilvejebringe tryk og temperatur.
Eksempel:
Lad os sige, at trykket er 1 pengeautomat, og temperaturen er 25 ° C (298K).
1. Konverter temperatur til Kelvin: 25 ° C + 273,15 =298,15 K
2. Sæt værdierne i formlen:
* n =(1 atm * 30 L) / (0,0821 L · ATM / Mol · K * 298,15 K)
* n ≈ 1,23 mol ilt
Derfor har du brug for tryk og temperatur for at bestemme antallet af mol ilt i 30L gas.
 Varme artikler
Varme artikler
-
 Brug af polymere membraner til at rense industrielle adskillelserZachary Smith er Joseph R Mares (1924) karriereudviklingsassistent professor i kemiteknik. Kredit:David Sella Der er snesevis af lovende teknologier under udvikling, der kan reducere energiforbrug
Brug af polymere membraner til at rense industrielle adskillelserZachary Smith er Joseph R Mares (1924) karriereudviklingsassistent professor i kemiteknik. Kredit:David Sella Der er snesevis af lovende teknologier under udvikling, der kan reducere energiforbrug -
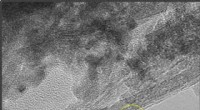 Bryde kæden - katalysere en grøn fremtid for kemiFig.1:TEM-billede af CeO2-understøttede ruthenium-nanopartikler katalysator. Gule cirkler viser Ru nanopartikler. Kredit:Osaka University Osaka Universitets forskere skaber katalysator til raffine
Bryde kæden - katalysere en grøn fremtid for kemiFig.1:TEM-billede af CeO2-understøttede ruthenium-nanopartikler katalysator. Gule cirkler viser Ru nanopartikler. Kredit:Osaka University Osaka Universitets forskere skaber katalysator til raffine -
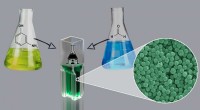 Kemikere udvikler metode til at opnå katalysator-, overfladeaktive og skabelonfrie polymere nanopar…Reaktion udviklet af RUDN -kemikere indeholder to monomerer - 3 -aminophenol og formaldehyd. Kredit:Allen Dressen En kemiker fra RUDN foreslår en simpel teknologi til fremstilling af polymere nano
Kemikere udvikler metode til at opnå katalysator-, overfladeaktive og skabelonfrie polymere nanopar…Reaktion udviklet af RUDN -kemikere indeholder to monomerer - 3 -aminophenol og formaldehyd. Kredit:Allen Dressen En kemiker fra RUDN foreslår en simpel teknologi til fremstilling af polymere nano -
 Billig, miljøvenlig katalysator åbner nye muligheder for organiske molekyler bygget af pyruvatPh.d.-studerende og førsteforfatter, Santanu Mondal, skitserer en reaktion af pyruvat ved at bruge en model af hans nydesignede organiske katalysatorsystem som reference. Kredit:OIST Kemikere ved O
Billig, miljøvenlig katalysator åbner nye muligheder for organiske molekyler bygget af pyruvatPh.d.-studerende og førsteforfatter, Santanu Mondal, skitserer en reaktion af pyruvat ved at bruge en model af hans nydesignede organiske katalysatorsystem som reference. Kredit:OIST Kemikere ved O
- Materialeforskere bruger stimuleret Raman -spredningsmikroskopi til at observere ioner, der bevæger…
- Første menneskelige migration ud af Afrika mere geografisk udbredt end tidligere antaget
- Online undervisning udløser en anden reaktion i kroppen
- Hvor længe varer orkidéblomstring? Tips til dyrkning af orkideer
- Hvorfor er granit godt for kerbstones?
- Knæk hvordan kokain virker


