Hvad er forskellen mellem atomer af carbon -12 og -14?
* carbon-12 (¹²c): Har 6 protoner og 6 neutroner. Dette er den mest almindelige isotop af kulstof, der udgør ca. 98,9% af alt carbon fundet naturligt.
* carbon-14 (¹⁴c): Har 6 protoner og 8 neutroner. Det er en radioaktiv isotop, hvilket betyder, at dens kerne er ustabil og nedbrydes over tid. Dette gør det nyttigt til radiocarbon -datering.
Her er en oversigt over de vigtigste forskelle:
| Funktion | Carbon-12 (¹²c) | Carbon-14 (¹⁴c) |
| ---------------- | ----------------- | ----------------- |
| Antal protoner | 6 | 6 |
| Antal neutroner | 6 | 8 |
| atommasse | 12 | 14 |
| Radioaktiv | Nej | Ja |
| overflod | 98,9% | ~ 1 del pr. Billion |
| halveringstid | Stabil | 5.730 år |
Kortfattet: Både carbon-12 og carbon-14 er isotoper af kulstof, hvilket betyder, at de har det samme antal protoner (atomnummer), men adskiller sig i antallet af neutroner. Carbon-14 er radioaktiv og nedbrydes over tid, mens Carbon-12 er stabil. Denne forskel i deres nukleare struktur fører til deres forskellige anvendelser inden for forskellige områder.
Sidste artikelHvad består fosfortrifluorid af?
Næste artikelHvad er elektronkonfigurationen til kobber?
 Varme artikler
Varme artikler
-
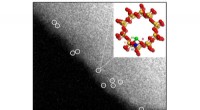 En måde at omdanne metan direkte til methanol eller eddikesyre under milde forholdAberrationskorrigerede HAADF/STEM-billeder af asyntetiseret Rh-ZSM-5. Enkelt rhodiumkationer er omkranset i hvidt med foreslået bold-stick-model af strukturen. Kredit:Lawrence F. Allard, medforfatter
En måde at omdanne metan direkte til methanol eller eddikesyre under milde forholdAberrationskorrigerede HAADF/STEM-billeder af asyntetiseret Rh-ZSM-5. Enkelt rhodiumkationer er omkranset i hvidt med foreslået bold-stick-model af strukturen. Kredit:Lawrence F. Allard, medforfatter -
 Dekonstruktion af superfooden, der bestemmer honningbiernes hierarkiKredit:CC0 Public Domain Alle bilarver spiser royal gelé, når de er nye, men kun fremtidige dronninger fortsætter med at spise det. For at finde ud af hvorfor, forskere i Østrig ser nærmere på de
Dekonstruktion af superfooden, der bestemmer honningbiernes hierarkiKredit:CC0 Public Domain Alle bilarver spiser royal gelé, når de er nye, men kun fremtidige dronninger fortsætter med at spise det. For at finde ud af hvorfor, forskere i Østrig ser nærmere på de -
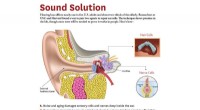 Tilslutning af hørehjælpemolekyler til øreknoglenKredit:USC Forskere ved USC og Harvard har udviklet en ny tilgang til at reparere celler dybt inde i øret - et potentielt middel, der kan genoprette hørelsen for millioner af ældre mennesker og an
Tilslutning af hørehjælpemolekyler til øreknoglenKredit:USC Forskere ved USC og Harvard har udviklet en ny tilgang til at reparere celler dybt inde i øret - et potentielt middel, der kan genoprette hørelsen for millioner af ældre mennesker og an -
 Forskere udvikler et strækkestativ til cellerElektronmikrofotografi af det tomme stillads (uden hydrogel), som et internationalt forskerhold brugte til at deformere individuelle celler. Kredit:Marc Hippler, SÆT Cellernes adfærd styres af der
Forskere udvikler et strækkestativ til cellerElektronmikrofotografi af det tomme stillads (uden hydrogel), som et internationalt forskerhold brugte til at deformere individuelle celler. Kredit:Marc Hippler, SÆT Cellernes adfærd styres af der
- Hvad er den største vulkan i Trinidad?
- Hvilket tidspunkt på dagen kan en solformørkelse ske?
- Hvordan kortlagde Newton Planets bane?
- Stråling kan komme fra solen og hvor ellers?
- Hvordan vi opdagede den mærkelige fysik af jetfly fra supermassive sorte huller
- Hvad genererer det, når du tørrer forbrænding af ethanol?


