Hvad er den afbalancerede ligning for aluminiumsulfatnatriumhydroxid?
al₂ (so₄) ₃ (aq) + 6naOH (aq) → 2al (OH) ₃ (s) + 3na₂so₄ (aq)
Her er en sammenbrud af reaktionen:
* reaktanter:
* aluminiumssulfat (al₂ (so₄) ₃) :En opløselig ionisk forbindelse.
* natriumhydroxid (NaOH) :En opløselig ionisk forbindelse.
* Produkter:
* aluminium hydroxid (AL (OH) ₃) :Et uopløseligt hvidt bundfald.
* natriumsulfat (na₂so₄) :En opløselig ionisk forbindelse.
Forklaring:
Denne reaktion er en dobbeltfortrængningsreaktion hvor kationerne og anionerne af reaktanterne skifter steder. Aluminiumioner (al³⁺) fra aluminiumsulfat reagerer med hydroxidioner (OH⁻) fra natriumhydroxid til dannelse af bundfaldet aluminiums hydroxid. De resterende ioner, natrium (Na⁺) og sulfat (SO₄²⁻), kombineres for at danne det opløselige natriumsulfat.
afbalancering af ligningen:
Ligningen er afbalanceret ved at sikre, at antallet af atomer i hvert element er det samme på begge sider af ligningen.
* aluminium (AL): 2 på begge sider
* svovl (er): 3 på begge sider
* ilt (O): 12 på begge sider
* natrium (NA): 6 På begge sider
* brint (H): 6 På begge sider
Denne afbalancerede ligning repræsenterer støkiometrien af reaktionen, hvilket indikerer proportioner af reaktanter og involverede produkter.
Sidste artikelHvor mange kovalente bindinger dannes af fluor?
Næste artikelHvad er de halve ligninger til rensning af kobber?
 Varme artikler
Varme artikler
-
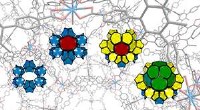 To simple byggeklodser producerer komplekst 3D-materialeSelvmontering af et metal-organisk stel. Kredit:Northwestern University Forskere fra Northwestern University har bygget et strukturelt komplekst materiale fra to simple byggesten, der er den metal
To simple byggeklodser producerer komplekst 3D-materialeSelvmontering af et metal-organisk stel. Kredit:Northwestern University Forskere fra Northwestern University har bygget et strukturelt komplekst materiale fra to simple byggesten, der er den metal -
 Bygninger – Beton på det dobbelteORNL forskere brugte fiberforstærkninger lavet af stål, glas og kulstof for at udvikle en betonblanding, der viste høj tidlig styrke inden for seks timer efter produktion, som er nødvendig for den præ
Bygninger – Beton på det dobbelteORNL forskere brugte fiberforstærkninger lavet af stål, glas og kulstof for at udvikle en betonblanding, der viste høj tidlig styrke inden for seks timer efter produktion, som er nødvendig for den præ -
 Detektering af et hidtil uset udvalg af potentielt skadelige luftbårne forbindelserDette bærbare badge i kreditkortstørrelse indeholder en ny type silica, der låser sig på en lang række VOCer. Kredit:Airotect Mange af de produkter, vi møder dagligt – fra deodorant til pesticider
Detektering af et hidtil uset udvalg af potentielt skadelige luftbårne forbindelserDette bærbare badge i kreditkortstørrelse indeholder en ny type silica, der låser sig på en lang række VOCer. Kredit:Airotect Mange af de produkter, vi møder dagligt – fra deodorant til pesticider -
 Undersøgelse afslører robust ydeevne i ældet detonatorsprængstofI skydekontrolrummet, postdoc-forsker Nicholas Lease (til højre), hænders forsknings- og udviklingsingeniør Nathan Burnside (i midten), et flashdrev til at overføre data til analyse, efter Maria Campb
Undersøgelse afslører robust ydeevne i ældet detonatorsprængstofI skydekontrolrummet, postdoc-forsker Nicholas Lease (til højre), hænders forsknings- og udviklingsingeniør Nathan Burnside (i midten), et flashdrev til at overføre data til analyse, efter Maria Campb
- Stemmegaffel
- Involverer horisontal kompressionsdeformation forkortelse og fortykning af skorpen?
- Hvordan arter dannes:Hvad den sammenfiltrede historie om forholdet mellem isbjørne og brunbjørne f…
- Hvad skal celler under udvikling for at udføre forskellige funktioner.?
- Held og lykke Mole - eksperimentet begynder at hamre ind i Mars-jorden
- Hvordan celler beskytter sig selv mod mitokondrielle defekter


