Hvad er elektronkonfigurationen af fluor?
1S² 2S² 2P⁶
Sådan ankommer vi til det:
* neutral fluor (F): Fluor har 9 elektroner. Dens elektronkonfiguration er 1S² 2s² 2p⁵.
* fluorion ion (f-): Fluor får en elektron for at opnå en fuld oktet og blive mere stabil. Denne ekstra elektron går ind i 2p orbital.
Derfor er den endelige elektronkonfiguration af fluorionionen 1S² 2S² 2P⁶.
Sidste artikelHvad er ladningen på stabil ion af vismut?
Næste artikelHvor mange atomer er der i et gram brint?
 Varme artikler
Varme artikler
-
 Forskellige teknikker er nødvendige for at opdage fingermærker på nye sedlerKredit:CC0 Public Domain Teknikker, der bruges til at opdage fingermærker på traditionelle bomuldssedler, er ikke effektive på skotske bankers nye polymernoter, og forskellige metoder er påkrævet,
Forskellige teknikker er nødvendige for at opdage fingermærker på nye sedlerKredit:CC0 Public Domain Teknikker, der bruges til at opdage fingermærker på traditionelle bomuldssedler, er ikke effektive på skotske bankers nye polymernoter, og forskellige metoder er påkrævet, -
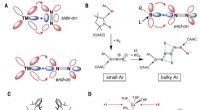 Forskere finder overraskende bindinger af overgangsmetal-typen, mens de bygger nye calcium(I)-komple…Nitrogenaktivering med overgangsmetaller (TM) eller bor og eksempler på lavvalente AE-metalkomplekser. Kredit: Videnskab (2021). DOI:10.1126/science.abf2374 Et team af forskere fra University Erl
Forskere finder overraskende bindinger af overgangsmetal-typen, mens de bygger nye calcium(I)-komple…Nitrogenaktivering med overgangsmetaller (TM) eller bor og eksempler på lavvalente AE-metalkomplekser. Kredit: Videnskab (2021). DOI:10.1126/science.abf2374 Et team af forskere fra University Erl -
 Video:Hvorfor muslingeskaller er hårdere end kridtKredit:The American Chemical Society Muslingeskaller består hovedsageligt af calciumcarbonat, også kendt som kridt, et mineral blødt og smuldrende nok til at kunne bruges til fortovskrabber. Alli
Video:Hvorfor muslingeskaller er hårdere end kridtKredit:The American Chemical Society Muslingeskaller består hovedsageligt af calciumcarbonat, også kendt som kridt, et mineral blødt og smuldrende nok til at kunne bruges til fortovskrabber. Alli -
 Karamelreceptor identificeretDen lugtende furaneol giver jordbær og andre fødevarer en karamellignende aroma. Figur:G. Olias / LSB, Figuren viser jordbær og strukturformlen for lugtstoffet furaneol. Kredit:G. Olias / LSB Hvem
Karamelreceptor identificeretDen lugtende furaneol giver jordbær og andre fødevarer en karamellignende aroma. Figur:G. Olias / LSB, Figuren viser jordbær og strukturformlen for lugtstoffet furaneol. Kredit:G. Olias / LSB Hvem
- Klimarelaterede katastrofer øger risikoen for konflikter i sårbare lande, viser forskning
- Strømafbrydelse lukker midlertidigt Amsterdams lufthavn
- Molekylære detaljer om proteinkrystalkernen afdækket
- Det mystiske Tully Monster-fossil er lige blevet mere mystisk
- USA overvejer at afslutte beskyttelsen af nordvestlige Montana-bjørne
- Hvor findes der en enkelt største masse vegetation?


