Hvor mange mol kuldioxid kan produceres fra 54 g ilt?
1. Skriv den afbalancerede kemiske ligning:
Forbrændingen af et carbonhydrid (som metan, CH4) producerer kuldioxid (CO2) og vand (H2O). Den afbalancerede ligning for forbrænding af metan er:
CH4 + 2O2 → CO2 + 2H2O
2. Bestem molforholdet:
Den afbalancerede ligning fortæller os, at 2 mol ilt (O2) er påkrævet for at producere 1 mol kuldioxid (CO2).
3. Konverter gram ilt til mol:
* Find den molære masse af ilt (O2):16 g/mol (O) * 2 =32 g/mol (O2)
* Opdel massen af ilt med dens molære masse:54 g / 32 g / mol =1,69 mol O2
4. Beregn mol CO2:
* Brug molforholdet fra den afbalancerede ligning:1,69 mol O2 * (1 mol CO2 / 2 mol O2) =0,845 mol CO2
Derfor kan 54 gram ilt producere 0,845 mol kuldioxid.
Sidste artikelHvad er 1 atom af kobbersvovl og 4 atomer ilt?
Næste artikelAntal elektroner i et neutralt atom -uran?
 Varme artikler
Varme artikler
-
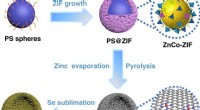 Team afslører en enkel metode til at producere højtydende lithium-selenbatterierSAC forberedelsesproces. Kredit: Naturkommunikation (2020). DOI:10.1038/s41467-020-18820-y Genopladelige lithium-ion-batterier (LIBer) betragtes som det bedste håb for næste generations batterite
Team afslører en enkel metode til at producere højtydende lithium-selenbatterierSAC forberedelsesproces. Kredit: Naturkommunikation (2020). DOI:10.1038/s41467-020-18820-y Genopladelige lithium-ion-batterier (LIBer) betragtes som det bedste håb for næste generations batterite -
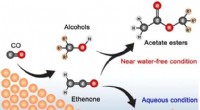 Bæredygtig elektrosyntese af estereVisual viser de processer, der er involveret i produktionen af C3 – C6 acetatestere fra den elektrokatalytiske reduktion af carbonmonoxid i en membranelektrodesamlingscelle. Kredit:Angewandte Chemie
Bæredygtig elektrosyntese af estereVisual viser de processer, der er involveret i produktionen af C3 – C6 acetatestere fra den elektrokatalytiske reduktion af carbonmonoxid i en membranelektrodesamlingscelle. Kredit:Angewandte Chemie -
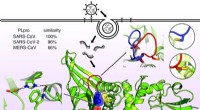 Information om molekylær form af vira, der forårsager COVID-19, SARS, og MERS afslører strukturel…Molekylær struktur af det papainlignende enzym kendt som PLPro. Dette enzym tillader de vira, der forårsager SARS, MERS, og COVID-19 for at inficere celler og replikere og undertrykke værtens immunfun
Information om molekylær form af vira, der forårsager COVID-19, SARS, og MERS afslører strukturel…Molekylær struktur af det papainlignende enzym kendt som PLPro. Dette enzym tillader de vira, der forårsager SARS, MERS, og COVID-19 for at inficere celler og replikere og undertrykke værtens immunfun -
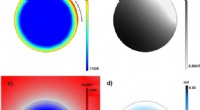 Udvikling af 3-D partikelmodel for enkeltpartikler i batterielektroderElektrokemiske fænomener inde i en enkelt partikel forudsagt ved hjælp af den udviklede model. a) Opladet tilstand; b) Elektrisk potentiale; c) Lithiumkoncentration; d) Spænding. Kredit:DGIST Der
Udvikling af 3-D partikelmodel for enkeltpartikler i batterielektroderElektrokemiske fænomener inde i en enkelt partikel forudsagt ved hjælp af den udviklede model. a) Opladet tilstand; b) Elektrisk potentiale; c) Lithiumkoncentration; d) Spænding. Kredit:DGIST Der
- Hvis de kræfter, der virker på et objekt, kan afbalanceres, kan ændre hastighedsretning eller gø…
- ATV Factory Tour
- Hvorfor har folk brug for videnskabelige eksperimenter?
- Tre hold finder en måde at måle frekvenser med langt bedre præcision end tidligere teknikker
- Efterligner naturen for programmerbare og adaptive syntetiske materialer
- Hvad er den lyseste obiect i himlen?


