En 2,14-L-prøve af hydrogenchlorid-HCl-gas ved 2,61 atm og 28C er fuldstændigt opløst i 668 ml vand til dannelse af saltsyreopløsning Beregn molariteten antager N?
1. Konverter temperatur til Kelvin:
* T (k) =t (° C) + 273.15
* T (k) =28 ° C + 273,15 =301,15 K
2. Brug den ideelle gaslov til at finde mol HCL:
* PV =NRT
* P =tryk (atm) =2,61 atm
* V =volumen (L) =2,14 L
* n =mol (mol)
*R =ideel gaskonstant =0,0821 l*atm/mol*k
* T =temperatur (k) =301,15 k
* Omarranger ligningen for at løse for N:
* N =PV / RT
* n =(2,61 atm * 2,14 l) / (0,0821 L * ATM / mol * K * 301,15 K)
* n ≈ 0,223 mol HCI
3. Beregn molariteten:
* Molaritet (m) =mol opløst / liter opløsning
* Mol opløst stof =0,223 mol HCl
* Liter opløsning =668 ml =0,668 L (husk at konvertere ML til L)
* M =0,223 mol HCI / 0,668 L
* M ≈ 0,334 m
Derfor er molariteten af hydrochlorsyreopløsningen ca. 0,334 m.
Sidste artikelHvad er fire metalliske ledere?
Næste artikelEr CaCl2 et rent stof eller en blanding?
 Varme artikler
Varme artikler
-
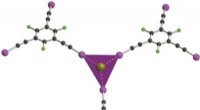 Koordinationskemi af anioner gennem halogenbindingsinteraktionerDetaljen af koordinationssfærerne af bromidanionen med Et3BuN+Br? Kredit:M. Fourmigué Mens en IUPAC-definition af hydrogenbinding først blev frigivet i 2011 efter årtiers diskussioner i det vide
Koordinationskemi af anioner gennem halogenbindingsinteraktionerDetaljen af koordinationssfærerne af bromidanionen med Et3BuN+Br? Kredit:M. Fourmigué Mens en IUPAC-definition af hydrogenbinding først blev frigivet i 2011 efter årtiers diskussioner i det vide -
 At bryde kuldioxid hurtigere, billigere, og mere effektivtEn opdagelse fra et team af forskere kunne gøre det mere muligt at omdanne kuldioxid til brændstoffer. Kredit:Steve Suib En ny katalysator nedbryder kuldioxid til nyttige kemikalier hurtigere, bil
At bryde kuldioxid hurtigere, billigere, og mere effektivtEn opdagelse fra et team af forskere kunne gøre det mere muligt at omdanne kuldioxid til brændstoffer. Kredit:Steve Suib En ny katalysator nedbryder kuldioxid til nyttige kemikalier hurtigere, bil -
 Børns modvilje mod blomkål, broccoli kunne skrives i deres mikrobiomKredit:CC0 Public Domain Mange børn, såvel som voksne, kan ikke lide Brassica grøntsager, såsom broccoli, blomkål, kål og rosenkål. I munden, enzymer fra disse grøntsager og fra bakterier i spyt
Børns modvilje mod blomkål, broccoli kunne skrives i deres mikrobiomKredit:CC0 Public Domain Mange børn, såvel som voksne, kan ikke lide Brassica grøntsager, såsom broccoli, blomkål, kål og rosenkål. I munden, enzymer fra disse grøntsager og fra bakterier i spyt -
 Molekylær blanding skaber superstabilt glasForsker Sandra Hultmark arbejder med en prøve af det nye glasmateriale ved hjælp af en FSC-maskine (Fast Scanning Calorimetry). Kredit:Sepideh Zokaei, Chalmers Tekniske Universitet Forskere ved Ch
Molekylær blanding skaber superstabilt glasForsker Sandra Hultmark arbejder med en prøve af det nye glasmateriale ved hjælp af en FSC-maskine (Fast Scanning Calorimetry). Kredit:Sepideh Zokaei, Chalmers Tekniske Universitet Forskere ved Ch


