Hvad er den komplette ioniske ligning for reaktion 2KOH (aq) H2SO4 (aq) 2H2O (i) K2SO4 (aq)?
2k⁺ (aq) + 2OH⁻ (aq) + 2H⁺ (aq) + so₄²⁻ (aq) → 2H₂O (l) + 2k⁺ (aq) + so₄²⁻ (aq)
Sådan ankommer vi til denne ligning:
1. Skriv den afbalancerede molekylær ligning:
2KOH (aq) + h₂so₄ (aq) → 2h₂o (l) + k₂so₄ (aq)
2. nedbryd de opløselige ioniske forbindelser i deres respektive ioner:
- Koh (aq) adskiller sig i k⁺ (aq) og OH⁻ (aq)
- H₂so₄ (aq) Dissocieres i 2H⁺ (aq) og so₄²⁻ (aq)
- K₂so₄ (aq) Dissocieres i 2K⁺ (aq) og so₄²⁻ (aq)
- H₂O (L) er en væske og adskiller sig ikke i ioner.
3.
2k⁺ (aq) + 2OH⁻ (aq) + 2H⁺ (aq) + so₄²⁻ (aq) → 2h₂o (l) + 2k⁺ (aq) + so₄²⁻ (aq)
Vigtig note: Den komplette ioniske ligning viser alle de ioner, der er til stede i opløsningen. Dette er forskelligt fra den nettoioniske ligning, der kun viser de ioner, der deltager i reaktionen (dem, der ændrer deres tilstand eller danner et bundfald).
 Varme artikler
Varme artikler
-
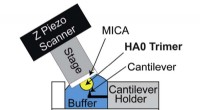 Virulensfaktor for influenza A-virus kortlagt i realtidHS-AFM opsætning til direkte visualisering af HA0 trimer. Skematisk diagram over HS-AFM-opsætningen til scanning af HA0-trimeren. Kredit:Kanazawa University Influenza A -vira, som tidligere er ans
Virulensfaktor for influenza A-virus kortlagt i realtidHS-AFM opsætning til direkte visualisering af HA0 trimer. Skematisk diagram over HS-AFM-opsætningen til scanning af HA0-trimeren. Kredit:Kanazawa University Influenza A -vira, som tidligere er ans -
 En squishy Rubiks Cube, som kemikere bygget af polymerer holder løfte om datalagringEn ny Rubiks Cube-lignende struktur lavet af en selvhelbredende hydrogel kan måske inspirere til nye måder at opbevare information på og muligvis hjælpe patienter med at overvåge deres medicinske tils
En squishy Rubiks Cube, som kemikere bygget af polymerer holder løfte om datalagringEn ny Rubiks Cube-lignende struktur lavet af en selvhelbredende hydrogel kan måske inspirere til nye måder at opbevare information på og muligvis hjælpe patienter med at overvåge deres medicinske tils -
 Blodprøver kan påvise tilstedeværelsen af dødelige superbugs på mindre end en timeElementer af det nye BYU-udviklede system til hurtig påvisning af superbugs i blod. Kredit:Claire Moore/BYU Photo Hvis du har antibiotika-resistente bakterier i dit blod, du skal vide ret hurtigt,
Blodprøver kan påvise tilstedeværelsen af dødelige superbugs på mindre end en timeElementer af det nye BYU-udviklede system til hurtig påvisning af superbugs i blod. Kredit:Claire Moore/BYU Photo Hvis du har antibiotika-resistente bakterier i dit blod, du skal vide ret hurtigt, -
 Forstå hvordan planter bruger sollysProfessor Gabriela S. Schlau-Cohen (i midten) og kandidatstuderende Raymundo Moya (til venstre) og Wei Jia Chen arbejdede med samarbejdspartnere på Verona Universitet, Italien, at udvikle en ny forstå
Forstå hvordan planter bruger sollysProfessor Gabriela S. Schlau-Cohen (i midten) og kandidatstuderende Raymundo Moya (til venstre) og Wei Jia Chen arbejdede med samarbejdspartnere på Verona Universitet, Italien, at udvikle en ny forstå
- Hvor findes Silver Tree Fern?
- Kombination af lys, superledere kan øge AI -mulighederne
- At vælge en partner:hvad vi virkelig ønsker
- Halvledere med en justeret grænseflade
- G20 finansierer fossile brændstoffer 30 milliarder dollars om året under radaren:analyse
- Undgå usikkerhedsprincippet i kvantefysik


