Hvor mange gram fast bariumhydroxid er nødvendige for nøjagtigt at neutralisere 14,7 ml A 0,597 M perchlorsyreopløsning?
1. Skriv den afbalancerede kemiske ligning:
Ba (OH) ₂ (aq) + 2hclo₄ (aq) → Ba (clo₄) ₂ (aq) + 2H₂O (l)
2. Beregn molen af perchlorsyre (HCLO₄):
* Molaritet (M) =mol (mol) / volumen (L)
* Mol HCLO₄ =molaritet × Volumen =0,597 m × 0,0147 l =0,00876 mol
3. Bestem molforholdet fra den afbalancerede ligning:
* Den afbalancerede ligning viser, at 1 mol Ba (OH) ₂ reagerer med 2 mol HCLO₄.
4. Beregn molen af bariumhydroxid (BA (OH) ₂):
* Mol Ba (OH) ₂ =(mol HCLO₄) / 2 =0,00876 mol / 2 =0,00438 mol
5. Beregn massen af bariumhydroxid:
* Masse (g) =mol (mol) × molmasse (g/mol)
* Molmasse BA (OH) ₂ =137,33 g/mol + 2 (17,01 g/mol) =171,35 g/mol
* Masse BA (OH) ₂ =0,00438 mol × 171,35 g/mol = 0,750 g
Derfor har du brug for 0,750 gram fast bariumhydroxid for nøjagtigt at neutralisere 14,7 ml af en 0,597 m perchlorsyreopløsning.
Sidste artikelHvad sker der, når alkylhalogenid reagerer med sølvnitrat?
Næste artikelHvilken type binding dannes mellem brom og brom?
 Varme artikler
Varme artikler
-
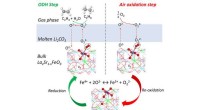 Katalysator åbner døren til mere effektiv, miljøvenlig produktion af ethylenReaktionsveje til oxidativ dehydrogenering af ethan lettet af den smeltede carbonatskal modificerede perovskit redox katalysator. Kredit:Fanxing Li, NC State University Et forskerhold ledet af Nor
Katalysator åbner døren til mere effektiv, miljøvenlig produktion af ethylenReaktionsveje til oxidativ dehydrogenering af ethan lettet af den smeltede carbonatskal modificerede perovskit redox katalysator. Kredit:Fanxing Li, NC State University Et forskerhold ledet af Nor -
 Ny forbindelse kan forbedre fotodynamisk terapi mod kræftKredit:CC0 Public Domain Forskere ved University of Sheffield har syntetiseret en ny forbindelse, der kan forbedre succesraten for fotodynamisk terapi ved behandling af kræft. Nøglen til fotodyna
Ny forbindelse kan forbedre fotodynamisk terapi mod kræftKredit:CC0 Public Domain Forskere ved University of Sheffield har syntetiseret en ny forbindelse, der kan forbedre succesraten for fotodynamisk terapi ved behandling af kræft. Nøglen til fotodyna -
 Ny 3D-printet sensor kan registrere glyphosat i drikkevarerIngeniører testede sensorenheden på prøver af appelsinjuice, som de tilsatte glyphosat til undersøgelsen. Kredit:Bob Hubner, Washington State University En nyudviklet, lavprissensor kan registrere
Ny 3D-printet sensor kan registrere glyphosat i drikkevarerIngeniører testede sensorenheden på prøver af appelsinjuice, som de tilsatte glyphosat til undersøgelsen. Kredit:Bob Hubner, Washington State University En nyudviklet, lavprissensor kan registrere -
 Forbedret menneskelig kropsreaktion på implantaterKredit:pixabay UPM-forskere har udviklet en ny overfladebehandling for at reducere afstødning af metalliske biomaterialeimplantater. Dette vil forlænge protesens levetid og dermed øge livskvalitet
Forbedret menneskelig kropsreaktion på implantaterKredit:pixabay UPM-forskere har udviklet en ny overfladebehandling for at reducere afstødning af metalliske biomaterialeimplantater. Dette vil forlænge protesens levetid og dermed øge livskvalitet
- Forurening fra døde Ivy League laboratoriemus bekymrer nabolaget
- Hvad er forskellene mellem en indfaldende stråle og en reflektionsstråle?
- Kaldes stoffer i slutningen af reaktionen reaktanter?
- Har vi fuldmåne i aften"?
- Hvordan tester man for tilstedeværelse af ammoniumion?
- Samsung viklet ind i One China-rækken, efter at K-pop-stjerne trækker sig


