Hvad sker der, når EDTA tilsættes til en opløsning af ammoniak og kobbersulfat?
Forståelse af komponenterne:
* kobbersulfat (cuso₄): Et blåt krystallinsk fast stof, der opløses i vand for at danne en blå opløsning, der indeholder kobber (II) -ioner (Cu²⁺).
* ammoniak (NH₃): En farveløs gas, der opløses i vand for at danne en svag base. Når ammoniak tilsættes til en kobbersulfatopløsning, danner den en kompleks ion med kobber, hvilket skaber en dyb blå farve. Dette skyldes dannelsen af tetraamminecopper (II) -ioner, [Cu (NH₃) ₄] ²⁺.
* edta (ethylendiaminetetraeddikesyre): Et kraftfuldt chelateringsmiddel. Det har seks bindingssteder, der kan koordinere med metalioner og danne et meget stabilt kompleks.
reaktionen:
1. starttilstand: Du har en opløsning, der indeholder kobber (II) -ioner kompleks med ammoniak, [Cu (NH₃) ₄] ²⁺.
2. edta tilføjelse: Når EDTA tilføjes, konkurrerer den med ammoniak til koordinering til kobber (II) -ioner.
3. Kompleks dannelse: EDTA danner et meget stabilt kompleks med kobber (II) -ioner, [Cu (EDTA)] ²⁻. Dette kompleks er så stabilt, at det effektivt fjerner kobber (II) -ioner fra opløsningen.
4. farveændring: Den dybe blå farve på [Cu (NH₃) ₄] ²⁺ -komplekset falmer, når kobberionerne sekvestreres af EDTA, der danner en farveløs eller lysblå opløsning.
generelt:
Tilsætningen af EDTA til en opløsning af ammoniak og kobbersulfat resulterer i dannelsen af et stabilt kobber-EDTA-kompleks, [Cu (EDTA)] ²⁻. Dette kompleks er så stærkt, at det fjerner kobber (II) -ioner fra opløsningen, hvilket fører til et fald i intensiteten af den blå farve.
Ansøgninger:
* Vandbehandling: EDTA bruges til at fjerne tungmetaller som kobber fra spildevand.
* Analytisk kemi: EDTA bruges i titreringer til at bestemme koncentrationen af metalioner.
* Medicin: EDTA bruges i chelationsterapi til at fjerne tungmetaller fra kroppen.
Bemærk: Den nøjagtige observerede farveændring kan afhænge af koncentrationen af reaktanterne. Hvis koncentrationen af kobbersulfat er høj, kan en svag blå farve vedvare, selv efter tilsætning af EDTA.
 Varme artikler
Varme artikler
-
 At finde kilden til kemiske reaktionerKredit:CC0 Public Domain Forskere søger konstant efter kilden til ting som universets oprindelse, materie eller liv. Forskere ved U.S. Department of Energys (DOE) Argonne National Laboratory, i et
At finde kilden til kemiske reaktionerKredit:CC0 Public Domain Forskere søger konstant efter kilden til ting som universets oprindelse, materie eller liv. Forskere ved U.S. Department of Energys (DOE) Argonne National Laboratory, i et -
 En ny idé forbinder syntesen af ler og stofskiftets oprindelseIllustration, der forbinder syntesen af lerarter og metabolismens oprindelse. Kredit:Ruixin Zhou Spørgsmålet om, hvordan livet er begyndt, har fascineret forskere fra mange discipliner, og det v
En ny idé forbinder syntesen af ler og stofskiftets oprindelseIllustration, der forbinder syntesen af lerarter og metabolismens oprindelse. Kredit:Ruixin Zhou Spørgsmålet om, hvordan livet er begyndt, har fascineret forskere fra mange discipliner, og det v -
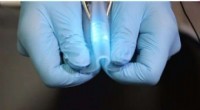 Sådan ser et stretchy kredsløb udForskere i Kina har lavet et nyt hybrid ledende materiale - del elastisk polymer, del flydende metal - der kan bøjes og strækkes efter ønske. Kredsløb lavet med dette materiale kan have de fleste todi
Sådan ser et stretchy kredsløb udForskere i Kina har lavet et nyt hybrid ledende materiale - del elastisk polymer, del flydende metal - der kan bøjes og strækkes efter ønske. Kredsløb lavet med dette materiale kan have de fleste todi -
 AI-drevet elektronisk næse til at opsnuse kødets friskhedE-næsen indeholder en stregkode, der ændrer farve på grund af reaktioner med gasser, der udsendes af det henfaldende kød, og en stregkodelæser i form af en smartphone-app drevet af AI, og er blevet tr
AI-drevet elektronisk næse til at opsnuse kødets friskhedE-næsen indeholder en stregkode, der ændrer farve på grund af reaktioner med gasser, der udsendes af det henfaldende kød, og en stregkodelæser i form af en smartphone-app drevet af AI, og er blevet tr


