Balance kemisk ligning af natriumchlorid plus kaliumiodid?
* opløselighed: Både natriumchlorid (NaCl) og kaliumiodid (KI) er meget opløselige i vand. Dette betyder, at de let opløses i deres ioner (Na+, Cl-, K+og I-), når de er i opløsning.
* Ingen drivkraft: Der er ingen stærk drivkraft for, at reaktionen forekommer. De produkter, der ville dannes, natriumiodid (NAI) og kaliumchlorid (KCL), er også meget opløselige og ville simpelthen forblive i opløsning som ioner.
Derfor ville den "kemiske ligning" for reaktionen se sådan ud:
NaCl (aq) + ki (aq) → Na + (aq) + cl- (aq) + k + (aq) + i- (aq)
I det væsentlige sker reaktionen ikke rigtig. Ionerne findes simpelthen i løsning sammen.
Fortæl mig, hvis du gerne vil udforske andre kemiske reaktioner!
Sidste artikelHvilken pH -værdi indikerer den højeste koncentration af hydroxidion?
Næste artikelHvordan har du kemisk netruliser CO2?
 Varme artikler
Varme artikler
-
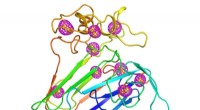 Ny tilgang til løsning af proteinstrukturer fra små krystallerEn tegneserie, der repræsenterer strukturen af et velstuderet planteprotein, der tjente som en testcase for den nyudviklede mikrokrystallografi teknik. Magenta maskemønstre, der omgiver svovlatomer,
Ny tilgang til løsning af proteinstrukturer fra små krystallerEn tegneserie, der repræsenterer strukturen af et velstuderet planteprotein, der tjente som en testcase for den nyudviklede mikrokrystallografi teknik. Magenta maskemønstre, der omgiver svovlatomer, -
 Forbindelser i en asiatisk fermenteret fiskepasta kan reducere højt kolesteroltalFermentering af karpefisk fører til frigivelse af forbindelser, der kan spille en rolle i at reducere kolesterolniveauet. Kredit:W.A. Djatmiko/C-C Wikimedia Forbindelser i en fermenteret fiskepast
Forbindelser i en asiatisk fermenteret fiskepasta kan reducere højt kolesteroltalFermentering af karpefisk fører til frigivelse af forbindelser, der kan spille en rolle i at reducere kolesterolniveauet. Kredit:W.A. Djatmiko/C-C Wikimedia Forbindelser i en fermenteret fiskepast -
 Konstruerede mikrober kan producere bionedbrydeligt plast til lavere omkostninger og miljøpåvirkni…Langt størstedelen af plastik er lavet af fossile brændstoffer, og nedbrydes ikke biologisk. Plastforurening hober sig op i vores have og vandveje, og mikroplast kommer i jorden, dyr, og endda vores
Konstruerede mikrober kan producere bionedbrydeligt plast til lavere omkostninger og miljøpåvirkni…Langt størstedelen af plastik er lavet af fossile brændstoffer, og nedbrydes ikke biologisk. Plastforurening hober sig op i vores have og vandveje, og mikroplast kommer i jorden, dyr, og endda vores -
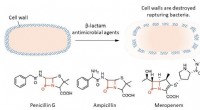 En ny synder i antibakteriel resistens:CysteinpersulfidØverst:β-lactam antimikrobielle midler sprænger bakterier ved at ødelægge deres cellevægge. Nederst:Den røde tekst i strukturformlen repræsenterer β-lactamringen, som er afgørende for bakteriedræbende
En ny synder i antibakteriel resistens:CysteinpersulfidØverst:β-lactam antimikrobielle midler sprænger bakterier ved at ødelægge deres cellevægge. Nederst:Den røde tekst i strukturformlen repræsenterer β-lactamringen, som er afgørende for bakteriedræbende


