Er RB F en ionisk eller kovalent binding?
* Elektronegativitetsforskel: Rubidium (RB) er et metal med en lav elektronegativitet, mens fluor (F) er en meget elektronegativ ikke -metal. Forskellen i elektronegativitet mellem dem er betydelig, hvilket fører til overførsel af et elektron fra rubidium til fluor.
* Dannelse af ioner: Rubidium mister en elektron for at blive en positivt ladet ion (RB+), mens fluor får en elektron for at blive en negativt ladet ion (F-).
* Elektrostatisk attraktion: De modsatte ladede ioner tiltrækker hinanden stærkt og danner en ionisk binding.
Kortfattet: Den store elektronegativitetsforskel mellem rubidium og fluor resulterer i dannelsen af ioner og deres elektrostatiske tiltrækning, der er karakteristisk for en ionisk binding.
 Varme artikler
Varme artikler
-
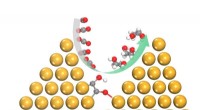 Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata
Super-selektive katalysatorer er nøglen til kulstofomdannelseDen unikke rumlige indeslutning induceret af kobbernanopyramider er afgørende for selektivt at generere ethylenglycol gennem en ny reaktionsvej. Kredit:Shizhang Qiao, Universitetet i Adelaide Kata -
 Forskere foreslår at bruge maskinlæring til at forudsige materialers egenskaberForskere foreslog at bruge maskinlæringsmetoder til at forudsige egenskaberne af kunstige safirkrystaller. Det er et unikt materiale, der er meget udbredt i mikroelektronik, optik og elektronik. Kredi
Forskere foreslår at bruge maskinlæring til at forudsige materialers egenskaberForskere foreslog at bruge maskinlæringsmetoder til at forudsige egenskaberne af kunstige safirkrystaller. Det er et unikt materiale, der er meget udbredt i mikroelektronik, optik og elektronik. Kredi -
 Binding af kuldioxid ved hjælp af knust betonNeustarks pilotanlæg forvandler knust beton og CO 2 til stengranulat, der kan tjene som erstatning for sand og grus i frisk beton. Kredit:Micha Riechsteiner Takket være teknologi fra ETH spin-of
Binding af kuldioxid ved hjælp af knust betonNeustarks pilotanlæg forvandler knust beton og CO 2 til stengranulat, der kan tjene som erstatning for sand og grus i frisk beton. Kredit:Micha Riechsteiner Takket være teknologi fra ETH spin-of -
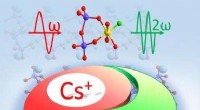 Forskning afdækker det første ikke-centrosymmetriske fluorooxosilicophosphat med Si-F-bindingerSkematisk illustration af forskningen. Kredit:Prof. LUOs gruppe Dyb-ultraviolette (UV) ikke-lineære optiske materialer spiller en afgørende rolle i en række forskellige højteknologiske videnskabel
Forskning afdækker det første ikke-centrosymmetriske fluorooxosilicophosphat med Si-F-bindingerSkematisk illustration af forskningen. Kredit:Prof. LUOs gruppe Dyb-ultraviolette (UV) ikke-lineære optiske materialer spiller en afgørende rolle i en række forskellige højteknologiske videnskabel
- Hvorfor er turgor -pres ikke et kendetegn ved dyreceller?
- Hvad er funktionerne for triglyceridphospholipid & sterol?
- Hvad er brændstofdesulfurisering?
- Sabeltandede katte og bjørnehunde:Hvordan de fik samlivet til at fungere
- Vil fluor og svovl danne ionforbindelse?
- Hvordan elektrokonvulsiv terapi virker


