Hvad er formålet med at tilføje NaCl -opløsning til sæbeblanding?
* sæbe er et salt: Sæbe fremstilles ved at reagere en fedtsyre med en stærk base (som NaOH eller KOH). Det resulterende produkt er et salt af denne fedtsyre.
* opløselighed: SOAP-molekyler har et polært "hoved" (saltdelen) og en ikke-polær "hale" (fedtsyrelen). Dette gør SOAP opløselig i både vand (polær) og fedt/olier (ikke-polær).
* Saltning af effekt: Når du tilsætter salt til sæbeblandingen, forstyrrer saltionerne balancen mellem de polære og ikke-polære dele af sæbe-molekylerne. Dette gør sæben mindre opløselig i vand og får den til at udfælde ud af opløsningen og danne en fast masse.
praktiske fordele ved at redde:
* adskillelse af sæbe: Salting ud giver dig mulighed for nemt at adskille sæben fra resten af blandingen (lut, vand, overskydende olier). Dette gør det lettere at rense og håndtere sæben.
* gør sæbe hårdt: Saltopløsningen hjælper også med at gøre sæben sværere og mere solid.
Kort sagt, tilføjelse af NaCl -opløsning til en sæbeblanding giver dig mulighed for at:
* Adskil sæbe
* gør sæben hårdere
Dette er et afgørende trin i traditionelle soapmaking -processer.
Sidste artikelHvad er pH på 1N natriumhydroxid?
Næste artikelEr opvaskemiddel en elementblandingsforbindelse eller rent stof?
 Varme artikler
Varme artikler
-
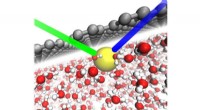 Den subtile rolle af overflader i ion-klæbrighedI vand (røde og hvide strukturer), den direkte interaktion mellem grafen (grå) og en thiocyanat (SCN‒) ion (gul) får ionen til at adsorbere til overfladen. De grønne og blå linjer repræsenterer indfal
Den subtile rolle af overflader i ion-klæbrighedI vand (røde og hvide strukturer), den direkte interaktion mellem grafen (grå) og en thiocyanat (SCN‒) ion (gul) får ionen til at adsorbere til overfladen. De grønne og blå linjer repræsenterer indfal -
 Tryk kan være nøglen til at bekæmpe klimaændringer med termoelektriske generatorerKunstners opfattelse af, hvordan påføring af tryk i diamantamboltcellen ændrer den elektroniske struktur af bly -selenid. Kredit:Xiao-Jia Chen Tryk forbedrer materialers evne til at omdanne varme
Tryk kan være nøglen til at bekæmpe klimaændringer med termoelektriske generatorerKunstners opfattelse af, hvordan påføring af tryk i diamantamboltcellen ændrer den elektroniske struktur af bly -selenid. Kredit:Xiao-Jia Chen Tryk forbedrer materialers evne til at omdanne varme -
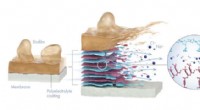 Afskalningsbelægning holder afsaltningen renere og grønnereDen aftagelige polyelektrolytbelægning forhindrer bioforurening på afsaltningsmembraner og undgår behovet for skadelige kemikalier til rengøring af havvandssaltningssystemer. Kredit:© 2020 KAUST; Xavi
Afskalningsbelægning holder afsaltningen renere og grønnereDen aftagelige polyelektrolytbelægning forhindrer bioforurening på afsaltningsmembraner og undgår behovet for skadelige kemikalier til rengøring af havvandssaltningssystemer. Kredit:© 2020 KAUST; Xavi -
 Undersøgelse viser, at zinks oxidationstilstand kan laves +3, fundamentalt ændre grundstoffernes k…Kredit:Unsplash/CC0 Public Domain Zink har traditionelt en valens på to, hvilket betyder, at to elektroner deltager i grundstoffets kemiske reaktion. Et nyt papir af Virginia Commonwealth Universi
Undersøgelse viser, at zinks oxidationstilstand kan laves +3, fundamentalt ændre grundstoffernes k…Kredit:Unsplash/CC0 Public Domain Zink har traditionelt en valens på to, hvilket betyder, at to elektroner deltager i grundstoffets kemiske reaktion. Et nyt papir af Virginia Commonwealth Universi


