Hvor mange atomer i 1 gram uran?
1. Find den molære masse af uran:
* Den molære masse af uran (U) er ca. 238,03 g/mol. Dette betyder 1 mol uran vejer 238,03 gram.
2. Konverter gram til mol:
* Opdel massen af uran (1 gram) med dens molære masse:
1 g / 238,03 g / mol =0,00420 mol
3. Brug Avogadros nummer:
* Avogadros nummer fortæller os, at der er 6,022 x 10²³ atomer i en mol af ethvert stof.
* Multiplicer antallet af mol uran (0,00420 mol) med Avogadros nummer:
0,00420 mol * 6,022 x 10²³ atomer/mol =2,53 x 10²¹ atomer
Derfor er der cirka 2,53 x 10²¹ atomer i 1 gram uran.
Sidste artikelNatrium na 11 stabil eller radioaktiv?
Næste artikelHvordan skriver du formelenheden til natriumiodid?
 Varme artikler
Varme artikler
-
 Undersøgelse sporer hjernens indre funktion med ny biosensorANU-lektor Colin Jackson (til venstre) var en af de førende forskere i denne undersøgelse. Kredit:Stuart Hay, ANU Et internationalt hold af forskere har taget et vigtigt skridt i retning af at f
Undersøgelse sporer hjernens indre funktion med ny biosensorANU-lektor Colin Jackson (til venstre) var en af de førende forskere i denne undersøgelse. Kredit:Stuart Hay, ANU Et internationalt hold af forskere har taget et vigtigt skridt i retning af at f -
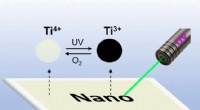 Skriv med lys på titaniumdioxid:Overskrivbare UV-følsomme overflader lavet af dopede TiO2 nanokrys…Grafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202203700 Det er lykkedes for forskere at fremstille et belægningsmateriale, der kan skrives på ved hjælp a
Skriv med lys på titaniumdioxid:Overskrivbare UV-følsomme overflader lavet af dopede TiO2 nanokrys…Grafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202203700 Det er lykkedes for forskere at fremstille et belægningsmateriale, der kan skrives på ved hjælp a -
 Automatisk syntese giver mulighed for opdagelse af uventet ladningstransportadfærd i organiske mole…Automatiseret synteseplatform i Molecule Marker Lab. Kredit:University of Illinois Urbana-Champaign Et tværfagligt team fra University of Illinois i Urbana-Champaign (UIUC) har demonstreret et stor
Automatisk syntese giver mulighed for opdagelse af uventet ladningstransportadfærd i organiske mole…Automatiseret synteseplatform i Molecule Marker Lab. Kredit:University of Illinois Urbana-Champaign Et tværfagligt team fra University of Illinois i Urbana-Champaign (UIUC) har demonstreret et stor -
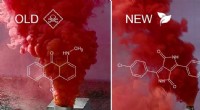 Et grønnere alternativ til rødfarvet røgFarvestoffer, der i øjeblikket bruges til rød røg (venstre), såsom det, der findes i blus, kan være giftige, så forskerne identificerede et sikrere alternativ (til højre). Kredit:Tilpasset fra ACS Sus
Et grønnere alternativ til rødfarvet røgFarvestoffer, der i øjeblikket bruges til rød røg (venstre), såsom det, der findes i blus, kan være giftige, så forskerne identificerede et sikrere alternativ (til højre). Kredit:Tilpasset fra ACS Sus


