Hvorfor forekommer reaktionen af jern og kobberchlorid?
Her er sammenbruddet:
* jern (Fe) er mere reaktiv end kobber (CU). Dette betyder, at jern har en stærkere tendens til at miste elektroner og danne positive ioner.
* Kobberchlorid (Cucl₂) indeholder kobberioner (Cu²⁺).
* Når jern tilsættes til en kobberchloridopløsning, desto mere reaktiv jern fortrænger jo mindre reaktivt kobber. Jernatomer mister elektroner og danner jern (II) -ioner (Fe²⁺), og kobberionerne får elektroner til at blive kobberatomer (Cu).
Dette er repræsenteret af følgende kemiske ligning:
Fe (s) + Cucl₂ (aq) → fecl₂ (aq) + cu (s)
Nøglepunkter:
* reaktionen er spontan Fordi det frigiver energi (eksotermisk).
* du vil observere Et rødbrunt fast stof (kobber), der dannes på overfladen af jernet, når reaktionen skrider frem. Løsningen ændrer også farve, når jernchloridformerne.
Denne reaktion er et klassisk eksempel på, hvordan reaktivitetsserier kan bruges til at forudsige resultatet af kemiske reaktioner.
Sidste artikelHvad er vandigt sølvnitrat og kaliumbromid kombineres for at danne et bundfald?
Næste artikelHvilke metaller ruster ikke?
 Varme artikler
Varme artikler
-
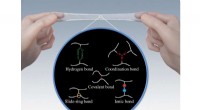 Elastomerer udvikler stærkere bindingsbindingerForskellige former for bindinger kan forbinde elastomerkæder sammen, ændre hvordan materialet opfører sig. Kredit:Yukikazu Takeoka Elastomerer er de bløde, elastiske materialer, som geler og gummi
Elastomerer udvikler stærkere bindingsbindingerForskellige former for bindinger kan forbinde elastomerkæder sammen, ændre hvordan materialet opfører sig. Kredit:Yukikazu Takeoka Elastomerer er de bløde, elastiske materialer, som geler og gummi -
 Koordineringspolymerer med op til 99,99% antibakteriel effektivitetKredit:RUDN University En kemiker ved RUDN University har sammen med sine kolleger fra Portugal udviklet to typer belægninger baseret på nye koordineringspolymerer med sølv. Begge forbindelser ble
Koordineringspolymerer med op til 99,99% antibakteriel effektivitetKredit:RUDN University En kemiker ved RUDN University har sammen med sine kolleger fra Portugal udviklet to typer belægninger baseret på nye koordineringspolymerer med sølv. Begge forbindelser ble -
 Ny teknik muliggør rumlig adskillelse af peptidstrukturerForskellige 3D-strukturer af biologiske molekyler, for eksempel et dipeptid med to forskellige konformationer vist som rødt og blåt, kan rumligt adskilles ved at skyde en kold molekylær stråle gennem
Ny teknik muliggør rumlig adskillelse af peptidstrukturerForskellige 3D-strukturer af biologiske molekyler, for eksempel et dipeptid med to forskellige konformationer vist som rødt og blåt, kan rumligt adskilles ved at skyde en kold molekylær stråle gennem -
 Årsager til beton- og asfaltforringelse forklaretEt nærbillede af en bro, viser forringet asfaltbelægning og beton. Kredit:Akihiro Moriyoshi Forskere har afsløret, at forringelsen af moderne beton- og asfaltstrukturer skyldes tilstedeværelsen
Årsager til beton- og asfaltforringelse forklaretEt nærbillede af en bro, viser forringet asfaltbelægning og beton. Kredit:Akihiro Moriyoshi Forskere har afsløret, at forringelsen af moderne beton- og asfaltstrukturer skyldes tilstedeværelsen
- Designbehandling af avancerede metaller, der producerer bedre skulptur
- Guancherne stammer fra Nordafrika, viser DNA-undersøgelse
- Hvad er 38,5 C i Fahrenheit?
- Hvad er to systemer involveret i koordineringen af menneskets krops funktion?
- Hvor kan man se månen mest tydeligt på nattehimlen?
- Sprogstudie udforsker, hvordan boksetrænere kommunikerer under pres


