Hvad er vandigt sølvnitrat og kaliumbromid kombineres for at danne et bundfald?
Her er den afbalancerede kemiske ligning for reaktionen:
Agno₃ (aq) + kBr (aq) → AgBr (s) + kno₃ (aq)
Forklaring:
* sølvnitrat (Agno₃) og kaliumbromid (KBR) er begge opløselige ioniske forbindelser, hvilket betyder, at de opløses i vand og findes som ioner.
* Når det er blandet, reagerer sølvionerne (Ag⁺) fra sølvnitrat med bromidionerne (BR⁻) fra kaliumbromid.
* Denne reaktion danner sølvbromid (AGBR) , som er uopløselig i vand og udfælder derfor som et fast stof.
* De resterende ioner, kalium (k⁺) og nitrat (no₃⁻), forbliver i opløsning som vandigt kaliumnitrat (kno₃) .
Nøglepunkter:
* Bundfaldet, sølvbromid , er et lysegult fast stof.
* Denne reaktion er et klassisk eksempel på en nedbørreaktion , hvor to opløselige ioniske forbindelser reagerer på dannelse af et uopløseligt produkt.
* Reaktionen drives af dannelsen af det uopløselige sølvbromid.
Sidste artikelHvor mange ioner er i 0,20 mol natriumchlorid?
Næste artikelHvorfor forekommer reaktionen af jern og kobberchlorid?
 Varme artikler
Varme artikler
-
 Din mad kan være med til at gøre mere klæbrig, sikrere lim til bærbare computere, emballage, mø…En gruppe videnskabsmænd ved Purdue University har hentet inspiration fra feltet, køkkenet og havet for at skabe stærke lime. Kredit:Purdue University Du kan ikke lave lim ud af en skinkesandwich
Din mad kan være med til at gøre mere klæbrig, sikrere lim til bærbare computere, emballage, mø…En gruppe videnskabsmænd ved Purdue University har hentet inspiration fra feltet, køkkenet og havet for at skabe stærke lime. Kredit:Purdue University Du kan ikke lave lim ud af en skinkesandwich -
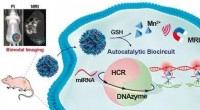 Amplifikation og billeddannelse af microRNA som en biomarkør for at påvise tumorudviklingKredit:Wiley-VCH/ Angewandte Chemie En god indikator for dysregulering i levende celler er en ændring i deres RNA -ekspression. MicroRNA (miRNA), en særlig type RNA, betragtes som en biomarkør f
Amplifikation og billeddannelse af microRNA som en biomarkør for at påvise tumorudviklingKredit:Wiley-VCH/ Angewandte Chemie En god indikator for dysregulering i levende celler er en ændring i deres RNA -ekspression. MicroRNA (miRNA), en særlig type RNA, betragtes som en biomarkør f -
 Selvdrevne papirspåner kunne hjælpe med at slå en tidlig alarm for skovbrandeEn sensor (hvid strimmel) på en stueplante aktiverer en alarm, når ilden er tæt på. Kredit:Tilpasset fra ACS anvendte materialer og grænseflader 2020 De seneste ødelæggende brande i Amazonas reg
Selvdrevne papirspåner kunne hjælpe med at slå en tidlig alarm for skovbrandeEn sensor (hvid strimmel) på en stueplante aktiverer en alarm, når ilden er tæt på. Kredit:Tilpasset fra ACS anvendte materialer og grænseflader 2020 De seneste ødelæggende brande i Amazonas reg -
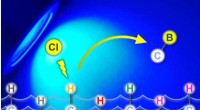 Ny tilgang inden for organisk kemi gør det muligt at tilføje bor til molekyler med høj præcisionEn simpel chloridkatalysator muliggør selektiv CH-borylering under milde fotokemiske forhold. Kredit:University of Bristol Et hovedmål inden for organisk syntese er at udvikle effektive reaktioner
Ny tilgang inden for organisk kemi gør det muligt at tilføje bor til molekyler med høj præcisionEn simpel chloridkatalysator muliggør selektiv CH-borylering under milde fotokemiske forhold. Kredit:University of Bristol Et hovedmål inden for organisk syntese er at udvikle effektive reaktioner
- Vi kunne finde udenjordiske civilisationer ved deres luftforurening
- 22 gamle amforer fundet ud for den albanske kyst
- Hvilke rejser i bølger selv gennem rummet?
- NASA estimerer den globale rækkevidde af atmosfæriske floder
- Hvad sker der med tyngdekraften, når massen stiger og afstand mellem genstande øges?
- Første, anden og tredje klasse Math Games


