Hvad er volumenet af svovldioxid SO2 -gas dannet, når 2 mol carbondisulfid CS2 brændes?
1. Skriv den afbalancerede kemiske ligning:
CS₂ (L) + 3O₂ (G) → CO₂ (G) + 2SO₂ (G)
2. Bestem molforholdet:
Den afbalancerede ligning viser, at 1 mol CS₂ producerer 2 mol SO₂.
3. Beregn molen af SO₂ produceret:
Da vi har 2 mol CS₂, kan vi bruge molforholdet til at finde mol på SO₂:
2 mol CS₂ * (2 mol SO₂ / 1 mol CS₂) =4 mol So₂
4. Antag STP (standardtemperatur og tryk) for at beregne volumen:
Ved STP (0 ° C og 1 atm) optager 1 mol af enhver ideel gas 22,4 L.
5. Beregn mængden af So₂:
4 mol SO₂ * (22,4 L/mol) = 89,6 L So₂
Derfor dannes 89,6 liter svovldioxidgas (SO₂), når 2 mol kulstofdisulfid (CS₂) brændes.
 Varme artikler
Varme artikler
-
 Modulerende spiralformede nanostrukturer i flydende krystalfase ved molekylært designKredit:Unsplash/CC0 Public Domain Et team af forskere ledet af adjunkt Yuki Arakawa (Toyohashi University of Technology, Japan) har med succes udviklet svovlholdige flydende krystal (LC) dimermole
Modulerende spiralformede nanostrukturer i flydende krystalfase ved molekylært designKredit:Unsplash/CC0 Public Domain Et team af forskere ledet af adjunkt Yuki Arakawa (Toyohashi University of Technology, Japan) har med succes udviklet svovlholdige flydende krystal (LC) dimermole -
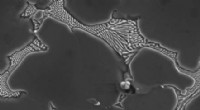 Varmehærdet magnesiumlegering et stærkt valg til implantaterBillede fra elektronmikroskop, der viser et stort bundfald i magnesiumlegering. Disse bundfald opløses ved varmebehandling, hvilket reducerer korrosionshastigheden væsentligt og gør legeringen meget s
Varmehærdet magnesiumlegering et stærkt valg til implantaterBillede fra elektronmikroskop, der viser et stort bundfald i magnesiumlegering. Disse bundfald opløses ved varmebehandling, hvilket reducerer korrosionshastigheden væsentligt og gør legeringen meget s -
 Væsen funktion:Vridende revner giver superhelte sejhed til dyrMantis-rejen erobrer sit bytte med et dactyl club vedhæng, som er opbygget af et kompositmateriale, der bliver sejere, efterhånden som revner vrider sig. Kredit:Purdue University billede/Pablo Zavatti
Væsen funktion:Vridende revner giver superhelte sejhed til dyrMantis-rejen erobrer sit bytte med et dactyl club vedhæng, som er opbygget af et kompositmateriale, der bliver sejere, efterhånden som revner vrider sig. Kredit:Purdue University billede/Pablo Zavatti -
 Forskere undersøger materialeegenskaber for længerevarende, mere effektive solcellerTidligere postdoktor ved Florida State University, Sarah Wieghold, venstre, og FSU adjunkt i kemi og biokemi Lea Nienhaus. Deres forskning hjælper med at forstå de grundlæggende processer i et materia
Forskere undersøger materialeegenskaber for længerevarende, mere effektive solcellerTidligere postdoktor ved Florida State University, Sarah Wieghold, venstre, og FSU adjunkt i kemi og biokemi Lea Nienhaus. Deres forskning hjælper med at forstå de grundlæggende processer i et materia
- Billede:Test af satellitmarkørdesign
- Hvad ser ud som mørke pletter i en måneformørkelse?
- Teknologi gør brændselsceller mere kraftfulde, mere holdbar, billigere
- Hvor mange mol luft er der i en 3L -beholder ved 1 atm -tryk og 293 K?
- Lyn og undersynlige udledninger producerer molekyler, der renser atmosfæren
- Hvornår er intensiteten af Suns -stråler størst?


