Hvordan dannes et natriumatombinding med kloratom?
forståelse af det grundlæggende
* natrium (NA): Natrium har en elektron i sin yderste skal (valensskal). Den ønsker at miste dette elektron for at opnå en stabil, fuld ydre skal som de ædle gasser.
* klor (Cl): Klor har syv elektroner i sin valensskal. Den ønsker at få et elektron for at afslutte sin ydre skal.
den ioniske bindingsdannelse
1. Elektronoverførsel: Natriumatomet overfører sin enkelt valenselektron til chloratomet.
2. Ioner dannelse:
* Natrium, efter at have mistet en elektron, har nu en positiv ladning og bliver en natriumion (Na+).
* Klor, efter at have fået en elektron, har nu en negativ ladning og bliver et chloridion (Cl-).
3. Elektrostatisk attraktion: De modsatte ladede ioner tiltrækker hinanden stærkt og danner en ionisk binding.
Resultatet:natriumchlorid (NaCl)
Den resulterende forbindelse, natriumchlorid, holdes sammen af den elektrostatiske tiltrækning mellem de positivt ladede natriumioner og de negativt ladede chloridioner. Denne attraktion er meget stærk, hvilket giver natriumchlorid sit karakteristiske høje smeltepunkt og en stærk krystallinsk struktur.
visuel repræsentation
Du kan visualisere denne proces som følger:
* na (en elektron i yderste skal) + cl (syv elektroner i det yderste skal)
* Na+ (tom yderste skal) + cl- (fuld yderste skal) -> NaCl (ionisk binding)
Nøglepunkter
* Ioniske bindinger involverer overførsel af elektroner, hvilket resulterer i dannelsen af ioner.
* Den elektrostatiske tiltrækning mellem modsat ladede ioner er drivkraften bag ionisk bindingsdannelse.
* Ioniske forbindelser er typisk faste stoffer ved stuetemperatur og har høje smeltepunkter.
Fortæl mig, hvis du har andre spørgsmål.
 Varme artikler
Varme artikler
-
 Forskere ser på måder at forbedre standard bremsesystemer påUBCO School of Engineering-forsker Mohammad Arjmand undersøger den nye polymerbaserede bremseklods, som kan revolutionere bremsesystemer i biler og tog. Kredit:UBC Okanagan Selvom det ikke er et s
Forskere ser på måder at forbedre standard bremsesystemer påUBCO School of Engineering-forsker Mohammad Arjmand undersøger den nye polymerbaserede bremseklods, som kan revolutionere bremsesystemer i biler og tog. Kredit:UBC Okanagan Selvom det ikke er et s -
 En motorvej for elektroner i oxidheterostrukturerFigur illustrerer vigtigheden af stærk (elektronisk) screening ved bestemmelse af elektronmobiliteten ved grænseflader af oxidheterostrukturer. Den betydelige forbedring af elektronmobilitet kan mul
En motorvej for elektroner i oxidheterostrukturerFigur illustrerer vigtigheden af stærk (elektronisk) screening ved bestemmelse af elektronmobiliteten ved grænseflader af oxidheterostrukturer. Den betydelige forbedring af elektronmobilitet kan mul -
 Uden for vægten:Fiskepanser både sejt og fleksibeltOptisk mikroskopibillede af tværsnittet af en karpeskala, der viser en flerlagsstruktur. Kredit:Quan et al., Struktur og mekanisk tilpasningsevne af en moderne Elasmoid fiskeskala fra almindelig karpe
Uden for vægten:Fiskepanser både sejt og fleksibeltOptisk mikroskopibillede af tværsnittet af en karpeskala, der viser en flerlagsstruktur. Kredit:Quan et al., Struktur og mekanisk tilpasningsevne af en moderne Elasmoid fiskeskala fra almindelig karpe -
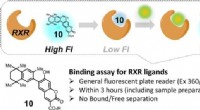 Syntetisk forbindelse giver hurtig screening for potentielle lægemidlerFluorescensen fra forbindelse 10 stiger, når en RXR-målretningsligand fortrænger den, hvilket gør det til en nyttig indikator for ligandaktivitet i assays. Kredit:Okayama University En simpel anal
Syntetisk forbindelse giver hurtig screening for potentielle lægemidlerFluorescensen fra forbindelse 10 stiger, når en RXR-målretningsligand fortrænger den, hvilket gør det til en nyttig indikator for ligandaktivitet i assays. Kredit:Okayama University En simpel anal
- Hvad er partiklerne i et solidt som folk, der sidder biograf?
- Samsung C-Labs gee-whiz resultater for at tegne udseende i Vegas
- Hvad hedder de sektioner af DNA, der kaldes under replikation?
- De etiske udfordringer ved digital identitet
- Heldig observation:Forskere ser et sort hul, der sønderdeler en stjerne
- Hvornår er det sikkert at ansætte en person med en straffeattest?


