Hvorfor gør atomer som kulstof og nitrogen ikke for at fremstille ioner, mens natriumchlor gør det?
Elektronegativitet og ioniseringsenergi
* Elektronegativitet: Dette måler et atoms evne til at tiltrække elektroner. Carbon og nitrogen har relativt høje elektronegativiteter, hvilket betyder, at de stærkt holder fast i deres egne elektroner. Natrium- og klor har henholdsvis meget lavere og højere elektronegativiteter.
* ioniseringsenergi: Dette er den energi, der kræves for at fjerne et elektron fra et atom. Carbon og nitrogen har høje ioniseringsenergier, hvilket gør det vanskeligt at fjerne et elektron til dannelse af en positiv ion (kation). Natrium har på den anden side en meget lav ioniseringsenergi, der let mister sin ydre elektron for at blive en positiv ion.
stabilitet af ioner
* kulstof og nitrogen: Når de forsøger at vinde eller miste elektroner til dannelse af ioner, er de resulterende ioner ustabile. F.eks. Er det nødvendigt, at kulstof får fire elektroner for at danne en -4 -ion. Dette ville skabe en meget negativ ladning, hvilket gør det meget reaktivt og usandsynligt at være stabilt.
* natrium og klor: Natrium mister let sin ene ydre elektron for at blive en stabil +1 -ion. Klor, med syv elektroner i dens ydre skal, får let et elektron for at opnå en stabil, fyldt ydre skal som en -1 -ion.
Bindingspræferencer
Carbon og nitrogen er mere tilbøjelige til at danne kovalente bindinger, hvor atomer deler elektroner. Denne deling giver begge atomer mulighed for at opnå en mere stabil elektronisk konfiguration.
Undtagelser:
* carbon Kan danne nogle ioniske forbindelser, men disse er sjældne og involverer normalt stærkt elektronegative elementer som fluor.
* nitrogen Kan danne ioniske forbindelser med metaller, men disse er også relativt usædvanlige.
Kortfattet:
Carbon og nitrogen foretrækker at dele elektroner gennem kovalent binding på grund af deres høje elektronegativitet, høj ioniseringsenergi og ustabiliteten af deres potentielle ioniske former. Natrium- og klor danner let ioner, fordi de opnår en stabil elektronkonfiguration ved at miste eller få elektroner.
Sidste artikelHvor mange atomer er der i 0,455 mol bly?
Næste artikelEr fluordas en elementforbindelse eller blanding?
 Varme artikler
Varme artikler
-
 Forudsige året i kemiKredit:CC0 Public Domain Med 2020 lige begyndt, forskere rundt om i verden undrer sig over, hvad året har i vente for dem. For at hjælpe med at styre dem lige, Kemi- og ingeniørnyheder ( C&EN
Forudsige året i kemiKredit:CC0 Public Domain Med 2020 lige begyndt, forskere rundt om i verden undrer sig over, hvad året har i vente for dem. For at hjælpe med at styre dem lige, Kemi- og ingeniørnyheder ( C&EN -
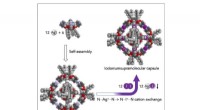 En ny hexamerisk molekylær kapsel i nanostørrelseEthylenbro-tetrakis (4-pyridyl) kavit og samler sig selv i en 4 nm oktaedrisk hexamer kapsel, når den behandles med sølvtosylat i chloroform. Kredit:Jyväskylä Universitet Haloniumioner brugt i den
En ny hexamerisk molekylær kapsel i nanostørrelseEthylenbro-tetrakis (4-pyridyl) kavit og samler sig selv i en 4 nm oktaedrisk hexamer kapsel, når den behandles med sølvtosylat i chloroform. Kredit:Jyväskylä Universitet Haloniumioner brugt i den -
 Økologiske polymerscintillatorer begejstrer røntgensamfundetAmorfe polymerscintillatorer, der udviser flere radioluminescensfarver, vil bidrage til røntgenbilleder i høj opløsning. Kredit:Wei et al., doi 10.1117/1.AP.4.3.035002. Røntgendetektion er af stor
Økologiske polymerscintillatorer begejstrer røntgensamfundetAmorfe polymerscintillatorer, der udviser flere radioluminescensfarver, vil bidrage til røntgenbilleder i høj opløsning. Kredit:Wei et al., doi 10.1117/1.AP.4.3.035002. Røntgendetektion er af stor -
 Undersøgelse beskriver cellulære fabrikker mere detaljeretKredit:CC0 Public Domain Mange vigtige naturlige produkter såsom antibiotika, immunsuppressiva og kræftlægemidler er afledt af mikroorganismer. Disse naturlige produkter er ofte små proteiner elle
Undersøgelse beskriver cellulære fabrikker mere detaljeretKredit:CC0 Public Domain Mange vigtige naturlige produkter såsom antibiotika, immunsuppressiva og kræftlægemidler er afledt af mikroorganismer. Disse naturlige produkter er ofte små proteiner elle
- Deadline for vestlige stater for at skære ned på Colorado-floden
- Når regeringer vedtager kunstig intelligens, der er lidt tilsyn og masser af fare
- Er kometer meteorer og asteroider navngivet?
- Hvor stor er solen sammenlignet med en stjerne?
- Hvordan ankom meteorer fra Mars på jorden?
- Hvad er 5 gram i ounces som en brøkdel?


