Hvilket har et højere smeltepunkt KCL eller HCI?
Forklaring:
* ionisk binding vs. kovalent binding: KCL er en ionisk forbindelse, mens HCL er en kovalent forbindelse. Ioniske forbindelser har stærke elektrostatiske attraktioner mellem modsat ladede ioner, som kræver en betydelig mængde energi for at overvinde. Kovalente forbindelser har svagere intermolekylære kræfter, såsom dipol-dipol-interaktioner eller London-spredningskræfter.
* gitterenergi: KCL har en høj gitterenergi på grund af de stærke elektrostatiske attraktioner mellem K+ og Cl- ioner. Denne høje gitterenergi gør det vanskeligt at bryde de ioniske bindinger og smelte forbindelsen.
* Polaritet: HCI er et polært molekyle, men dipol-dipolinteraktionerne mellem HCL-molekyler er meget svagere end de ioniske bindinger i KCL.
smeltepunkter:
* KCL:770 ° C (1418 ° F)
* HCI:-114,2 ° C (-173,6 ° F)
På grund af den stærke ioniske binding og høj gitterenergi har KCL derfor et signifikant højere smeltepunkt end HCI.
Sidste artikelEr svovlnatriumchlorid sand et fysisk eller kemikalie?
Næste artikelHvad er formlen for Mercury II -oxid?
 Varme artikler
Varme artikler
-
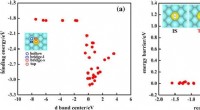 AI ledte efter enkeltatom-legeringskatalysatorer, fundet 200 lovende kandidaterFig. 1:Korrelation mellem simple deskriptorer og målegenskaber. Skoltech-forskere og deres kolleger fra Kina og Tyskland har præsenteret en ny søgealgoritme efter single-atom-legeringskatalysatore
AI ledte efter enkeltatom-legeringskatalysatorer, fundet 200 lovende kandidaterFig. 1:Korrelation mellem simple deskriptorer og målegenskaber. Skoltech-forskere og deres kolleger fra Kina og Tyskland har præsenteret en ny søgealgoritme efter single-atom-legeringskatalysatore -
 Miniproteiner, der kan lancere tostrengede angreb på virale proteinerDimerisering af spidsprotein med to-sidet peptid. Kredit:Bhavesh Khatri Den hurtige fremkomst af nye stammer af SARS-CoV-2-viruset har formindsket beskyttelsen fra COVID-19-vacciner. En ny tilgang
Miniproteiner, der kan lancere tostrengede angreb på virale proteinerDimerisering af spidsprotein med to-sidet peptid. Kredit:Bhavesh Khatri Den hurtige fremkomst af nye stammer af SARS-CoV-2-viruset har formindsket beskyttelsen fra COVID-19-vacciner. En ny tilgang -
 Jane Austen -citat kodet i en polymerEt citat fra Jane Austens Mansfield Park skrevet i oligourethanes. Kredit:Sarah Moor Ved hjælp af en ny molekylær datalagringsteknik, forskere ved University of Texas i Austin har kodet et citat f
Jane Austen -citat kodet i en polymerEt citat fra Jane Austens Mansfield Park skrevet i oligourethanes. Kredit:Sarah Moor Ved hjælp af en ny molekylær datalagringsteknik, forskere ved University of Texas i Austin har kodet et citat f -
 Nye molekyler til OLED'er og lægemidlerFotografi af opløsninger af syntetiserede thiophenderivater i dioxan i dagslys og bestråling med en UV -lampe med en excitationsbølgelængde på 380 nm. Kredit:Nataliya Belskaya, Professor, UrFU Institu
Nye molekyler til OLED'er og lægemidlerFotografi af opløsninger af syntetiserede thiophenderivater i dioxan i dagslys og bestråling med en UV -lampe med en excitationsbølgelængde på 380 nm. Kredit:Nataliya Belskaya, Professor, UrFU Institu


